Der AAMI HE 75 trägt den Titel „Human Factor Engineering – Design of Medical Devices”.
Erfahren Sie in diesem Artikel, was dessen Inhalte sind und wann Sie dieses mit 445 Seiten sehr umfangreiche Werk überhaupt lesen sollten. Damit können Sie (z.B. als Usability Engineer) entscheiden, ob sich der Kauf des AAMI HE 75 für $390 lohnt.
Anwendungsbereich, Ziele und Zielgruppe des AAMI HE 75
a) Zielgruppe: Hersteller, Anwender, Behörden, Lernende
Der AAMI HE 75 versteht sich als Nachschlagewerk und „Best Practice Guide“ zum Thema Usability bzw. Human Factors Engineering bei Medizinprodukten. Er wendet sich an Personen und Institutionen, die Medizinprodukte herstellen, prüfen und anwenden:
- Hersteller, die Benutzungsschnittstellen spezifizieren, entwickeln und verbessern
- Hersteller, die Benutzungsschnittstellen überprüfen und im Markt überwachen
- Krankenhäuser, die die Gebrauchstauglichkeit von Medizinprodukten bewerten
- Krankenhäuser, die Schwierigkeiten beim Umgang mit Medizinprodukten verstehen und verhindern möchten
- Behörden, Gesetzgeber oder benannte Stellen, die die Gebrauchstauglichkeit von Medizinprodukten beurteilen
- Studierende, die mehr über das Thema „Human Factors Engineering“ lernen möchten
Der HU 75 präsentiert sich somit als umfangreiches Lehrbuch und Nachschlagewerk zum Thema Usability.
b) Keine Einschränkung bezüglich des Typs von Medizinprodukten
Der Fokus des AAMI HE75 liegt zwar auf Medizinprodukten und damit auf spezifischen Aspekten wie dem Risikomanagement, den verwendeten Symbolen und dem speziellen Nutzungskontext. Allerdings sind viele der vorgestellten Prinzipien universell anwendbar.
Der HE 75 ist für alle Medizinprodukte anwendbar: Vom nicht-aktiven Produkt über komplexe Beatmungsgeräte bis hin zu Systemen aus Produkten und deren Zusammenspiel z.B. in der häuslichen Umgebung.
c) Verweis auf HE 74 zum “Usability Prozess”
Beim „Human factors design process for medical devices“ verweist der HE 75 auf den HE 74. D.h. der Usability-Engineering-Prozess ist nicht Gegenstand des HE 75. Letzterer konzentriert sich auf die Methoden und Verfahren des Usability Engineerings und schreibt nicht genau vor, welche Rolle in welcher Phase des Entwicklungsprozesses welche der Methoden/Verfahren anwendet.
Regulatorische Relevanz
Der Herausgeber des HE 75 ist die AAMI, die US-dominierte „Association for the Advancement of Medical Instrumentation“. Die AAMI-Dokumente haben keine gesetzliche Verbindlichkeit. Jedoch greift insbesondere die FDA auf das Wissen dieser „consensus standards“ zurück. Sie verwendet die Inhalte in eigenen Präsentationen (Beispiel) und verweist darauf im eigenen Guidance Dokument „Applying Human Factors and Usability Engineering to Medical Devices“.
Lesen Sie hier mehr über
Neben der FDA verweist auch die IEC 62366-2 auf den HE 75.
Wenn Sie konform mit dem HE 75 arbeiten, dürften Sie die regulatorischen Anforderungen in Europa und den USA erfüllen. In anderen Worten: Der HE 75 möchte nicht gesetzlich verbindlich sein (und darf das auch nicht), möchte aber beitragen, gesetzliche Anforderungen zu erfüllen.
Inhalt der AAMI HE 75
a) HE 75 im Überblick
Der HE 75 besteht aus vier großen Kapiteln, die in insgesamt 25 Abschnitte unterteilt sind:
- Das erste Kapitel definiert den Anwendungsbereich, Referenzen und Begriffe.
- Das zweite Kapitel stellt die allgemein gültigen Prinzipien vor: vom Design, über das Risikomanagement bis zum Testing und der nachgelagerten Phase.
- Das dritte Kapitel geht auf spezielle Elemente der Benutzungsschnittstelle wie Konnektoren und Software-Interfaces ein.
- Das vierte Kapitel diskutiert spezielle Produkttypen wie integrierte Systeme, mobile Anwendungen und Produkte für die häusliche Anwendung.
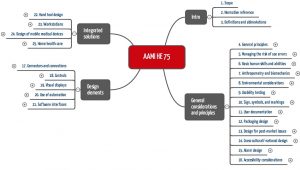
Dieser Beitrag stellt im Folgenden die einzelnen Abschnitte kurz vor. Sie können auch direkt zum Fazit springen.
b) Zusammenfassung der 25 Abschnitte
4. Abschnitt („General Principles“)
Dieser Abschnitt fasst die wichtigsten „Best Practices“ zusammen wie die Forderung, Geräte einfach und konsistent mit Gestaltungsregeln zu entwickeln. Die folgende Abbildung gibt eine Übersicht über diese Prinzipien:
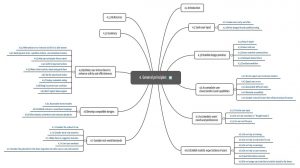
Bedauerlicherweise sagt der HF 75 nur, was man tun soll, aber nicht wie.
5. Abschnitt („Managing the risk of use error“)
Hier geht es darum, wie das Risikomanagement im Rahmen des Designs und der Bewertung der Gebrauchstauglichkeit umgesetzt werden kann. Damit „dekliniert“ der AAMI HE 75 die ISO 14971 mit Fokus auf Risiken aufgrund mangelnder Gebrauchstauglichkeit durch. Insbesondere die Kapitel 5.5 bis 5.15 folgen der Reihenfolge der Risikomanagementnorm:
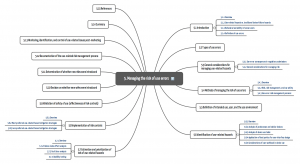
6. Abschnitt (“Basic human skills and abilities”)
Dieser Abschnitt beschreibt, wie Menschen mit Systemen umgehen, wie sie wahrnehmen, wie sie Informationen verarbeiten, diese verstehen, wie sie handeln und welche Fehler ihnen dabei unterlaufen.
7. Abschnitt (“Anthropometry and biomechanics”)
Im europäischen Sprachraum hätte man dieses Kapitel wahrscheinlich mit „Ergonomie“ überschrieben. Es geht um Größen, Positionen und Formen von Produkten, damit sie mit der Gestalt des menschlichen Körpers harmonieren. Der HE 75 diskutiert, wie man Daten wie z.B. zu Stärke und Beweglichkeit von Menschen erhebt und nutzt.
Hilfreich sind die Angaben typischer Größen wie die Länge von Extremitäten, der Durchmesser des Brustkorbs, die Höhe der Augen beim Sitzen, die Länge von Fingern u.v.m.
8. Abschnitt (“Environmental considerations”)
Die Gebrauchstauglichkeit ist keine universelle Eigenschaft, sondern abhängig von der Benutzungsumgebung. Dazu zählen die physische Umgebung (Helligkeit, Feuchtigkeit, Lärm, Druck, Temperatur) ebenso wie die mentale Umgebung (Stress, Hektik). Dies führt dieser Abschnitt aus.
9. Abschnitt (“Usability testing”)
Der HE 75 stellt in diesem Abschnitt zwar die Methoden vor, um Usability-Tests zu planen, durchzuführen, zu bewerten und zu dokumentieren. Dabei bezieht er sich jedoch auch auf den HE 74, so dass dieser Abschnitt in sich nicht ganz vollständig ist.
Das hier Beschriebene könnte man als Zusammenfassung dessen verstehen, was man beim CPUX-UT (Usability-Testing) Kurs lernt.
10. Abschnitt (“Signs, symbols, and making”)
Der Titel sagt bereits um was es geht: Labels, Aufschriften, Icons, Symbole und deren Größe, Reihenfolge und Nutzung. Auf diesen Abschnitt nehmen beispielsweise die Abschnitte 11 und 19 („Visual Displays“) Bezug.
11. Abschnitt („User documentation“)
Gleich, ob es um eine ausgedruckte, oder um eine elektronische, sogar multimediale Dokumentation geht: Dieser Abschnitt liefert Hinweise, die auch im folgenden Abschnitt Beachtung finden sollten. Dabei geht der HE 75 auf verschiedene Typen an Dokumentation ein wie „User Guides“, „Operator Manuals“ und „Quick-reference Guides“.
12. Abschnitt („Packing design“)
Wie soll man die Verpackung gestalten, dass man sie leicht nutzen kann, sie den Versand gut übersteht und die Medizinprodukte schützt? Dieser Abschnitt gibt Antworten.
13. Abschnitt („Design for post-market issues“)
Hier geht es nicht primär um die Marktüberwachung, sondern um die Phasen des Lebenszyklus nach der Entwicklung und Produktion: Wartung, Wiederverwendung und Entsorgung.
14. Abschnitt („Cross-cultural / cross-national design“)
Dass verschiedene Kulturkreise verschiedene Vorlieben, Konventionen und Erwartungen haben, die beim Design der Benutzungsschnittstelle beachtet werden sollten, lehrt der 14. Abschnitt. Er diskutiert beispielsweise die Bedeutung von Farben und Symbolen, hierarchische versus partnerschaftliche Arbeitskulturen und den Bezug zur Population und damit teilweise wieder zur Anthropologie (Abschnitt 7).
15. Abschnitt („Alarm design”)
Dieser Abschnitt hat den Anspruch, die Anforderungen der IEC 60601-1-8 zu ergänzen. Das betrifft Alarmsysteme, Warnsignale und vergleichbare Mechanismen. Auch wenn die IEC 60601-1-8 bereits sehr präzise Anforderungen stellt, ist dieser Abschnitt lesenswert.
16. Abschnitt („Accessibility considerations“)
Menschen mit vorrübergehenden oder dauerhaften körperlichen oder/und mentalen Einschränkungen haben spezielle Anforderungen. Medizinprodukte sollten daran adaptierbar sein. Der HE 75 geht auf die verschiedensten Aspekte ein wie Blindheit, Hörschwäche, Verlust der oberen oder unteren Extremitäten, Sprachschwierigkeiten und mangelnde Bereitschaft, sich ausreichend Zeit für die Nutzung des Produkts zu nehmen.
17. Abschnitt („Conectors and connections“)
Als erster Abschnitt im Kapitel “Design Elements” gibt dieser 17. Abschnitt Hinweise, wie Anschlüsse gestaltet werden sollten, um Vertauschungen oder nicht funktionierende Verbindungen von Produkten und Systemen zu vermeiden.
18. Abschnitt („Controls“)
Was man bei der Auswahl und Gestaltung von Steuerungen und Steuerungselementen beachten sollten, stellt dieser Abschnitt vor.
19. Abschnitt („Visual displays”)
Dieser Abschnitt gibt Hilfestellung bei der Technologieauswahl und der Gestaltung von visuellen Ausgaben.
20. Abschnitt („Use of automation“)
Probleme bei der Automatisierung, bei der Aufgabenzuteilung und beim Feedback durch das System beschreibt dieser Abschnitt – und gibt Anregungen zu deren Lösung.
21. Abschnitt („Software user interfaces“)
Der Titel dieses Abschnitts ist selbsterklärend. Hier beschreibt der HE 75 zum einen die Typen an Software-Interfaces vom kleinen LCD-Display bis zur mehrere Monitore übergreifenden Darstellung. Zum anderen nennt er allgemeine Anforderungen wie die Forderung, dass sie Nutzungsfehler vermeiden helfen sollen oder dass Information lesbar bleiben muss.
Im Unterabschnitt 21.4 wird das AAMI-Dokument konkreter. Es gibt Hinweise zu Schriftgrößen, zur Informationsarchitektur, zu Schriftarten, Farben und der Ausrichtung und Positionierung von Texten und UI-Elementen. Damit ist es teilweise redundant mit der ISO 9241-Familie.
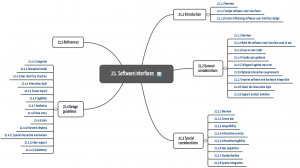
22. Abschnitt („Hand tool design“)
Hier geht es um die Gestaltung von Griffen und Handstücken. Dabei nimmt dieser Abschnitt Bezug zum siebten Abschnitt (“Anthropometry and biomechanics”).
23. Abschnitt („Workstations“)
Technisch orientierte Personen vermuten hinter dem Begriff „Workstations“ möglicherweise Computersysteme. Das trifft nicht zu. Dieser Abschnitt beschreibt Anforderungen an Arbeitsplätze, an Möbel, Materialien und Oberflächen. Dabei werden auch hier Bezüge zum siebten Kapitel mit der Ergonomie genommen.
24. Abschnitt („Design of mobile medical devices“)
Gegenstand sind weniger Mobile Medical Apps, sondern eher alle tragbaren Medizinprodukte. Deren (wechselnde) Nutzungsumgebungen (z.B. in Hubschraubern, Krankenwagen) stellen spezielle Anforderungen, die hier diskutiert werden.
25. Abschnitt (“Home health care”)
Die Besonderheiten der häuslichen Umgebung sind mannigfaltig. Dazu zählen beispielsweise die Benutzung der Produkte durch Laien und ggf. Menschen mit körperlichen und geistigen Einschränkungen.
Fazit
a) Redundante Enzyklopädie?
Der AAMI HE 75 präsentiert enzyklopädisches Wissen. Er steht damit teilweise in Konkurrenz zu Lehrbüchern (z.B. „Usability Engineering als Erfolgsfaktor, Effizient IEC 62366- und FDA-konform dokumentieren“), zu Normen (z.B. IEC 62366-2, ISO 9241-Familie) und zu anderen Best-Practice Guides (z.B. FDA Guidance Document). Er referenziert und ergänzt diese aber auch.
b) Etwas veraltet
Der AAMI HE 75 stammt aus dem Jahr 2009, wurde aber 2013 nochmals als aktuell bestätigt („reconfirmed“), ohne ihn tatsächlich zu aktualisieren. Das allermeiste hat in der Tat noch Gültigkeit. Einige Referenzen sind veraltet, die IEC 62366-2 kennt der HE 75 ebenso wenig wie die ISO 9241-210, die den Requirements- und Usability-Engineering-Prozess vorzüglich beschreibt.
Moderne Technologien, Plattformen und Trends wie die Mobile Apps kommen deutlich zu kurz.
c) Fehlende Handlungsleitung
Mit über 450 Seiten ist der HE 75 zu lang, um auf die Schnelle studiert zu werden. Bedauerlicherweise beschreibt der HE 75 meist nur, was getan werden muss, gibt aber keine konkrete Handlungsleitung, wie etwas getan werden könnte.
d) Empfehlung für die Verwendung
Andererseits enthält der AAMI HE 75 Informationen, die sonst mühsam in anderen Quellen recherchiert werden müssten, wie die Daten zur Anthropometrie oder zur interkulturellen Aspekten. Somit eignet er sich v.a. für (angehende) Usability Profis als Nachschlagewerk und als vertiefendes Lehrbuch, auf das sich auch die FDA gerne bezieht. Die Texte sind gut verständlich formuliert, und Bilder helfen, das Geschriebene noch schneller zu erfassen.
Als Lehrbuch für Studierende scheidet der HE 75 ob des (zu) hohen Preises aus.


Sehr geehrtes Johner Team,
Die ANSI wurde meines Wissens zuletzt 2018 neu publiziert. Ist der Punkt b aus dem Fazit hinsichtlich dem zu kurz kommen von aktuellen Trends, modernen Technologien und Plattformen weiterhin aktuell, oder wurde hier nachgebessert?
Sofern ein inhaltliches Update stattgefunden hat, wäre eine kurze Darstellung der aktuellen Inhalte bzw. Unterschiede zur Originalpublikation von 2009 sicherlich für Unternehmen interessant, die über eine Anschaffung der aktuellen Version nachdenken.
Sehr geehrter Herr Landgrebe,
besten Dank für die Anregung! Sie haben Recht, wir haben das Fazit noch nicht aktualisiert. Ich frage gleich bei unseren Usability-Kollegen nach und bitte diese, Ihnen zu antworten.
Mit den besten Grüßen
Christian Johner
Sehr geehrtes Johner Team,
inzwischen gibt es eine 2025 Ausgabe der HE75. Es wäre interessant, wenn dieser Artikel die Unterschiede davon aufzeigen könnte.
Das werden wir machen, lieber Herr Roth!
Danke für Ihren wichtigen Hinweis!
Beste Grüße, Christian Johner