CIRS sind seit Jahren im Gesundheitswesen und der Luftfahrt gesetzlich vorgeschrieben, um Meldungen über kritische Vorkommnisse anonym sammeln, auswerten und daraus Schlüsse für ein sichereres Arbeiten ziehen zu können. Bei Medizinprodukteherstellern sind CIRS keine Pflicht. Ein Fehler? Lesen Sie, wie Sie als Medizinproduktehersteller von CIRS profitieren können.
Was ein CIRS ist
Ein CIRS (Critical Incident Reporting System) ist ein oft papierbasiertes, meist elektronisches System, bei dem Mitarbeiter einer Organisation Beobachtungen zu Zwischenfällen oder Beinahe-Zwischenfällen anonym melden können.
Oft geben die meldenden Personen auch konkrete Hinweise zur Problemursache sowie Lösungsvorschläge.
Die Organisation wertet die Meldungen systematisch aus und zieht entsprechende Konsequenzen – nicht für den Meldenden sondern für die eigene Organisation z.B. in Form von
- überarbeitenden Prozessen,
- Steigerung von Kompetenzen und Bewusstsein,
- Einsatz von Technologien, um ähnliche Fehler zu vermeiden.
Welche Vorteile ein CIRS bringt
Allgemein
Ein CIRS kann dazu beitragen, mehr über die Fehlerentstehung zu verstehen und entsprechende Maßnahmen zu ergreifen:
- Abschätzen von Wahrscheinlichkeiten:
Ein CIRS hilft, die Anzahl von Ereignissen besser abzuschätzen und statistisch auszuwerten. Teilweise verfügen Organisationen über keine weiteren und für Ihre Organisation spezifischen belastbaren Zahlen. - Finden von Fehlerursachen
Nur wenn Informationen über Fehler vorliegen, kann man eine systematische Ursachenanalyse betreiben. - Identifizieren von Verbesserungsmaßnahmen
Die Maßnahmen dienen primär der Reduktion von Risiken. Allerdings finden sich in den Meldungen häufig Hinweise zur Verbesserung der Organisation unabhängig vom Risikomanagement. - Steigern der Fehlerkultur
Wenn Mitarbeiter erfahren, dass Meldungen nicht sanktioniert werden, sondern wichtig für die eigene Organisation sind und zu direkter Verbesserung führen, wird sich eine Kultur breit machen, in der Fehler nicht mehr verheimlicht, sondern als Anlass verstanden werden, Dinge fortlaufend zu verbessern.
Anwendungsmöglichkeiten eines CIRS bei Medizinprodukteherstellern
Auch Medizinproduktehersteller können von den CIRS profizieren:
- Arbeitsschutz
Wie in jeder Firma bestehen v.a. in der Produktion Sicherheitsrisiken, die mit Hilfe eines CIRS systematisch erfasst und minimiert werden können. - Risikomanagement: Abschätzen von Wahrscheinlichkeiten
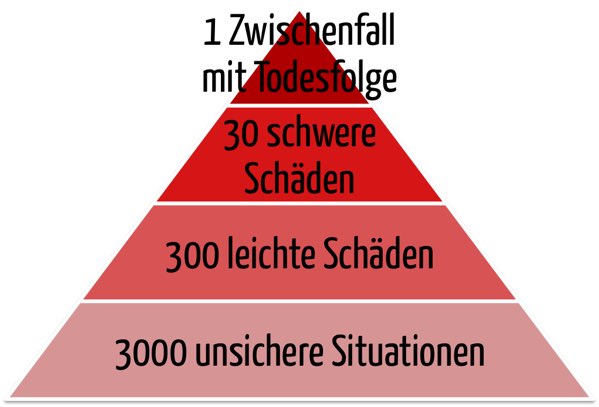
Die Zahlen wie die von DuPont (s. Abb.) helfen bei der Risikoanalyse dabei, die Wahrscheinlichkeiten von verschiedenen Schweregraden besser abzuschätzen. Wenn beispielsweise während eines Jahres drei Patienten leichte Schäden durch das Medizinprodukt erlitten, lässt sich aus der CIRS-Pyramide ableiten, dass die Wahrscheinlichkeit eines Todesfalls durch die gleiche Fehlerursache innerhalb dieses Jahres bei 1% liegt. - Klinische Bewertung
Bei der klinischen Bewertung anhand von Literaturdaten stehen die Hersteller oft vor der Herausforderung, dass in der klinischen Literatur im Kontext Risiko und Zwischenfälle nur sehr schwere Probleme insbesondere Todesfälle analysiert und publiziert wurden. Mit Hilfe der CIRS-Pyramide können Hersteller daraus die Wahrscheinlichkeiten für geringere Schweregrade extrapolieren.
Voraussetzungen für einen erfolgreichen Einsatz eines CIRS
Ein CIRS wird nur dann zum Erfolg, wenn die Organisationen einige generelle Spielregeln einhalten:
- Anonymität und Vertrauen: Die Anonymität muss gewahrt bleiben. Andernfalls kann sich die Organisation das Vertrauen nicht erarbeiten, das notwendig ist, um eine Fehlerkultur zu etablieren, in der jeder nicht bekannte Fehler als verpasste Chance verstanden wird.
- Freiwilligkeit: Sie können Menschen nicht zwingen. Laden Sie sie ein, teilzunehmen und die gemeinsame Organisation zu verbessern.
- Umsetzung: Nur über Verbesserung zu reden, bringt nichts. Sie müssen Meldungen regelmäßig (typisch ist ein monatliches oder vierteljährliches Intervall) nicht nur lesen und auswerten, sondern Maßnahmen ergreifen.
- Kommunikation: Sprechen Sie über die Maßnahmen – aber nicht über die Personen (s. Anonymität). Wenn Ihre Mitarbeiter erfahren, dass Ihre Meldungen Beachtung finden und zur Verbesserung beitragen, werden sie häufiger und präziser melden.
- Einfachheit: Halten Sie den Prozess und die Tools einfach. Vermeiden Sie aufwendige Bildschirmmasken und Formulare. Ein unbeobachteter Briefkasten, in dem man etwas einwerfen kann, ein auf der Webseite gut verlinktes Eingabeformular genügen.
Fazit
Ich möchte Medizinproduktehersteller ermutigen
- ein eigenes CIRS einzuführen (ggf. zusammen mit einem betrieblichen Vorschlagswesen) und
- bestehende CIRS-Daten systematisch für das Risikomanagement und die klinische Bewertung zu nutzen.

Sehr geehrte Damen und Herren,
ist es möglich, dass mir Kontaktdaten von Schulungsexperten oder Dozenten mit
dem Schwerpunkt CIRS schicken könnten?
Wir möchten in unserer Klinik CIRS Schulungen und Informationsschulungen
durch einen externen Anbietern durchführen.
Herzlichen Dank für Ihre Hilfe!