MEDDEV-Dokumente sind von der EU-Kommission veröffentlichte Leitlinien für insbesondere Medizinproduktehersteller und Benannte Stellen.
Vorsicht: Die MEDDEV-Dokumente sind (weitgehend) obsolet!
Mit der Ablösung der EU-Richtlinien MDD, AIMDD und IVDD durch die EU-Verordnungen MDR und IVDR sind die MEDDEV-Dokumente weitgehend obsolet. Eine Ausnahme bildet beispielsweise die Leitlinie MEDDEV 2.7/1 rev 4.
Hersteller und Benannte Stellen sollten daher immer prüfen, ob es eine passende MDCG-Leitlinie gibt.
Bitte beachten Sie dazu den Überblicksartikel zu den MDCG-Leitlinien und die dort verlinkten MEDDEV-Dokumente!

1. Inhalte der MEDDEV-Dokumente
Die MEDDEV-Dokumente decken mehrere Themenbereiche ab:
a) Anwendung der Richtlinien
- MEDDEV 2.1/1: Definitionen der Begriffe Medizinprodukt, Zubehör und Hersteller
- MEDDEV 2.1/2: Anwendungsbereich der AIMD-Richtlinie
- MEDDEV2.1/3: Borderline-Produkte, z. B. Produkte für die Verabreichung von Medikamenten
- MEDDEV 2.1/4: Schnittstellen mit anderen Richtlinien, z. B. solchen mit Bezug zur elektromagnetischen Verträglichkeit (89/336/EEC) und Schutzausrüstung (89/686/EEC)
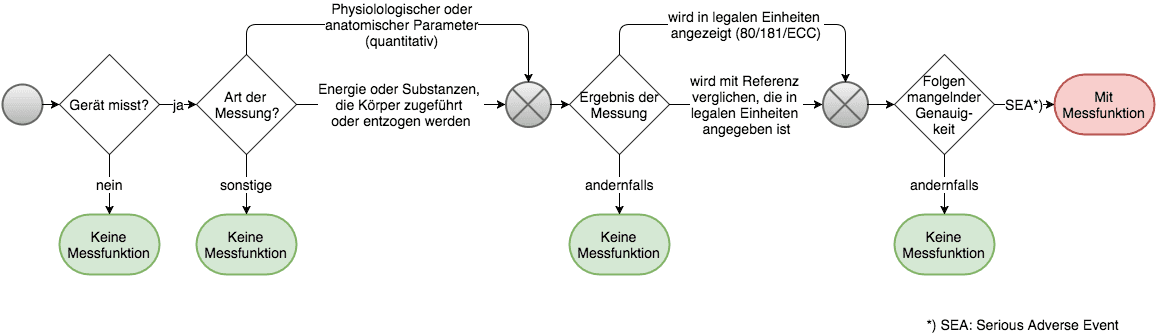
- MEDDEV 2.1/5: Medizinprodukte mit Messfunktionen
- MEDDEV 2.1/6: Klassifizierung von Standalone-Software als Medizinprodukt
b) Grundlegende Anforderungen
- MEDDEV 2.2/1: Elektromagnetische Verträglichkeit
- MEDDEV 2.2/3: Ablauf-/Mindesthaltbarkeitsdatum
- MEDDEV 2.2/4: Konformitätsbewertung bei In-vitro-Fertilisation
c) Klassifizierung von Medizinprodukten
- MEDDEV 2.4/1: Klassifizierung von Medizinprodukten (gemäß Anhang IX der MDD)
d) Konformitätsbewertungsverfahren
- MEDDEV 2.5/3: QM-Systeme mit Bezug zu Unterauftragnehmern
- MEDDEV 2.5/5: Übersetzungen
- MEDDEV 2.5/6: Verifizierung von „Batches“
- MEDDEV 2.5/7, /9 und /10: Konformitätsbewertung spezieller Produkte
e) Klinische Bewertung und klinische Prüfung
- MEDDEV 2.7/1: Klinische Bewertung: Hinweise für Hersteller und Benannte Stellen
- MEDDEV 2.7/2: Hinweise für kompetente Behörden bei der Bewertung klinischer Prüfungen
- MEDDEV 2.7/3: Klinische Prüfungen: Meldung von Zwischenfällen
- MEDDEV 2.7/4: Richtlinien für klinische Prüfungen: Hinweise für Hersteller und Benannte Stellen
f) Benannte Stellen
- MEDDEV 2.10: Ernennung und Überwachung von Benannten Stellen (nicht: durch Benannte Stellen)
g) Marktüberwachung
- MEDDEV 2.12/1: Richtlinien für ein Medizinprodukteüberwachungssystem
- Es gibt ausfüllbare PDFs und andere Formulare, z. B. für die Dokumentation von Zwischenfällen, korrektiven Maßnahmen, Meldungen an Kunden.
- MEDDEV 2.12/2: Klinische Studien zur Marktüberwachung (Post-Market Clinical Follow-up)
h) In-vitro-Diagnostika
- MEDDEV 2.14/1: Klassifizierung von Borderline-Produkten
- MEDDEV 2.14/2: IVD ausschließlich zu Forschungszwecken
- MEDDEV 2.14/3: Bedienungsanleitungen für IVD
- MEDDEV 2.14/4: CE-Kennzeichnung von blutbasierten IVD
Eine vollständige Übersicht über die Dokumente finden Sie auf der Webseite der EU.
2. Wer an den MEDDEV-Dokumenten mitwirkt
An der Erstellung der MEDDEV-Dokumente wirken (offiziell) mit:
- EU-Kommission
- Benannte Stellen
- Industrievertreter
- Behörden, z. B.:
- für Deutschland: Vertreter der ZLG, des Gesundheitsministeriums und seiner Behörden, insbesondere das BfArM und das Paul-Ehrlich-Institut
- für die Schweiz: Swissmedic
- für Österreich: das Bundesgesundheitsministerium
- Sonstige Interessensgruppen wie die Normungsgremien und Lobbyisten
3. Bewertung der MEDDEV-Dokumente
Die MEDDEV-Dokumente unterstützen Hersteller dadurch, dass sie die regulatorischen Vorgaben (insbesondere die der Richtlinien) weiter konkretisieren. Allerdings gibt es auch Kritik an diesen Dokumenten:
- Undemokratischer(?) und intransparenter Prozess
Der Prozess, in dem die Dokumente entstehen, ist intransparent und langwierig, sodass die direkt betroffene Medizinprodukteindustrie nur schwer daran mitwirken kann.
- Mangelnde Ausgewogenheit
In dem Gremium gibt es keine Vertreter von Patienteninteressen.
- Unklare rechtliche Verbindlichkeit
Die rechtliche Verbindlichkeit ist unklar: Manche Benannten Stellen bewerten Firmen auf Basis der MEDDEV-Dokumente, auch wenn diese Dokumente tendenziell über die Forderungen der Richtlinien hinausgehen oder nur eine von mehreren Interpretationen der EU-Richtlinien beinhalten.
- Veraltete Forderungen
Die MEDDEV-Dokumente sind teilweise veraltet. Eine Überarbeitung wird seit Jahren angekündigt, ohne sichtbares und endgültiges Ergebnis. Teilweise werden Dokumente referenziert, die längst nicht mehr gelten. Dieselbe Kommission fordert von den Herstellern, den Stand der Technik einzuhalten.
- Zusätzlicher Aufwand
Die MEDDEV-Dokumente erhöhen den Aufwand von Medizinprodukteherstellern bei der Einarbeitung in die regulatorische Landschaft.
- Kompensation eines unzureichenden Rechtssystems?
Dass das europäische Rechtssystem überhaupt der MEDDEV-Dokumente bedarf, macht klar, dass die Richtlinien nicht ausreichend präzise und vollständig sind.
Unter Software als Medizinprodukt (Software as Medical Device, SaMD) versteht man (eigenständige) Standalone-Software, die ein Medizinprodukt ist, aber nicht Teil eines solchen. Sie ist nicht zu verwechseln mit Medical Device Software im Sinne der EU. Wann müssen Sie als Hersteller Software als Medizinprodukt und wann als Medical Device Software qualifizieren? Das erfahren Sie hier – und können…
Details
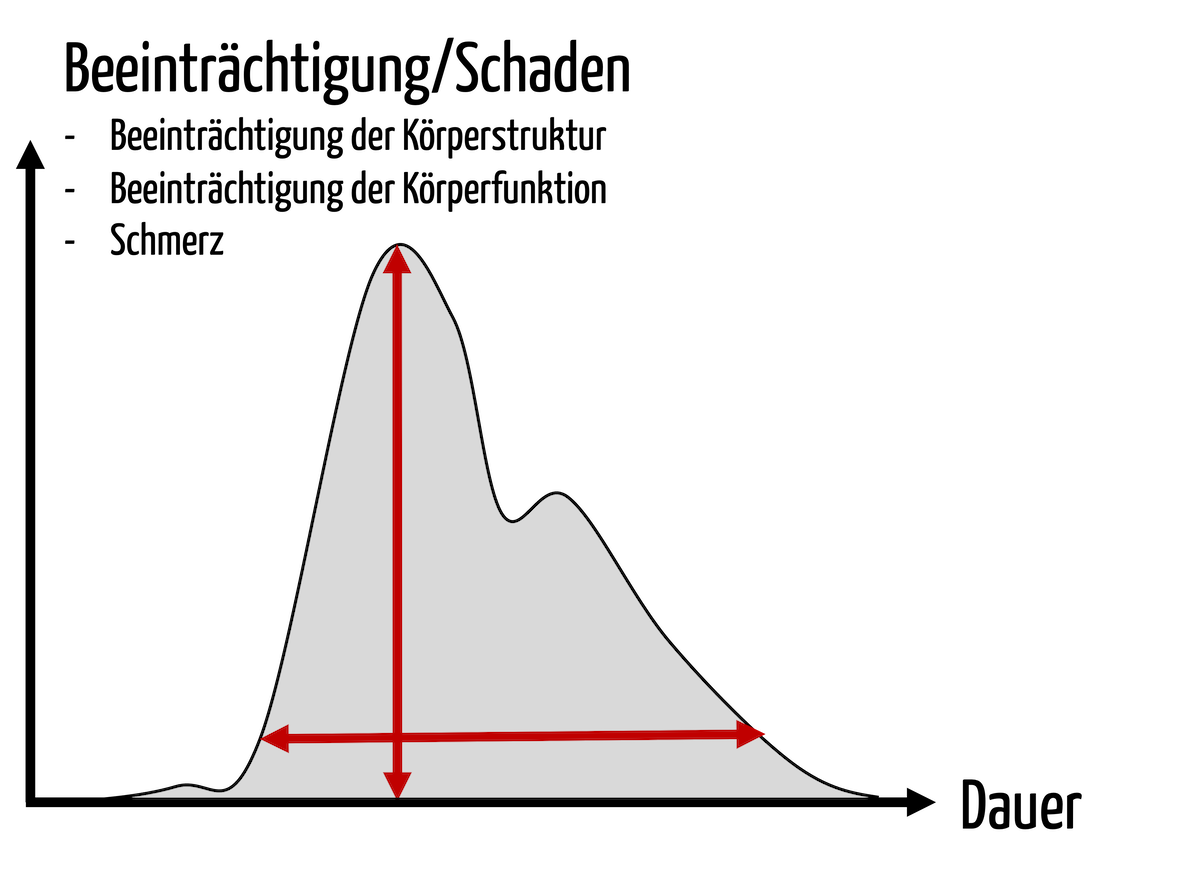
Medizinproduktehersteller müssen die Schweregrade möglicher Schäden bestimmen, um die Risiken durch ihre Produkte bewerten zu können. Was sich einfach anhört, ist in der Praxis sehr herausfordernd. Dieser Artikel gibt Hilfestellung, um die Schweregrade dieser Schäden ISO 14971-konform zu bestimmen und zu dokumentieren.
Details
Die MEDDEV 2.12-1 beschreibt die Anforderungen der EU an ein Marktüberwachungs- und Meldesystem (Vigilanz-System). Dieses Vigilanz-System ist Gegenstand von ISO-13485- bzw. Anhang-II-Zertifizierungsaudits.
Medizinprodukte mit Messfunktion sind etwas Besonderes. Wichtig (u.a.): Messfunktion beeinflusst die Klassifizierung. Doch nicht alles, was misst, hat eine Messfunktion. Bei der Einordnung hilft die MEDDEV 2.1./5.
Dieser Beitrag konzentriert sich auf Kommunikationsserver im Krankenhaus bzw. im Gesundheitswesen, beschreibt deren Aufgaben und die regulatorischen Anforderungen, die Hersteller und Betreiber (z.B. Krankenhäuser) erfüllen müssen. Kommunikationsserver: Zu was sie dienen Die Kommunikationsserver dienen der Vermittlung von Daten zwischen zwei Endpunkten wie IT-Systemen oder Medizinprodukte. Dazu müssen sie folgende Aufgaben erfüllen:
Details