Die Medical Device Regulation (MDR) ist eine EU-Verordnung, die Hersteller einhalten müssen, die Medizinprodukte in der EU in den Verkehr bringen wollen. Sie betrifft auch Händler und Importeure dieser Produkte sowie Benannte Stellen.
Die Verordnung (EU) 2017/745 über Medizinprodukte, so der offizielle Titel der MDR, trat bereits 2017 in Kraft und gilt seit dem 26. Mai 2021.
Einstieg in die EU Medical Device Regulation schaffen
Medizinproduktehersteller
Einen ersten Überblick über die Medical Device Regulation verschafft Ihnen dieser Fachartikel zur MDR. Das darin verlinkte Video stellt Ihnen die EU-Medizinprodukteverordnung in wenigen Minuten vor. Weiterhin finden Sie dort:
- Die wichtigsten Anforderungen der MDR
- Aufbau und Struktur der Verordnung
- Weiterführende Informationen, z. B. zu den Übergangsfristen
Andere Akteure
Falls Sie kein Medizinproduktehersteller sind, sollten Sie mit diesen Seiten starten:
Unten auf dieser Schlagwortseite finden Sie alle weiteren Fachartikel zur MDR.
Unterstützung bei der Umsetzung der MDR 2017/745
a) Kostenfreie Angebote
Haben Sie noch Fragen zur MDR und zu deren Umsetzung? Antworten erhalten Sie in unserem kostenlosen Micro-Consulting.
Laden Sie sich das kostenlose Starter-Kit herunter. Es verschafft Ihnen einen Überblick über die regulatorische Landschaft und zeigt die 6 Schritte zur „Zulassung“ Ihres Medizinprodukts. Außerdem enthält es die MDR-Checkliste als PDF und im DOCX-Format!
b) Videos und E-Learning
Die Videotrainings im Auditgarant zeigen Ihnen Schritt für Schritt, wie Sie Ihre Technische Dokumentation und Ihr QM-System sowohl schlank und schnell als auch MDR-konform erstellen. Dazu stehen über 100 Templates und Musterdokumente zum Download bereit.
So schaffen Sie die Voraussetzungen, um Ihre Produkte schnell und sicher zuzulassen und in den Markt zu bringen.
c) Prüfung
Die Expertinnen und Experten des Johner Instituts helfen Ihnen beim Prüfen Ihrer Produkte:
d) Beratung
Nutzen Sie das Knowhow unserer Regulatory Affairs Experts, um Ihre
Nehmen Sie gleich Kontakt auf, damit wir gemeinsam klären können, wie Sie die regulatorischen Anforderungen der EU Medizinprodukteverordnung MDR schnell und einfach erfüllen und Ihre Produkte sicher in den Markt bringen.
Kontakt aufnehmen
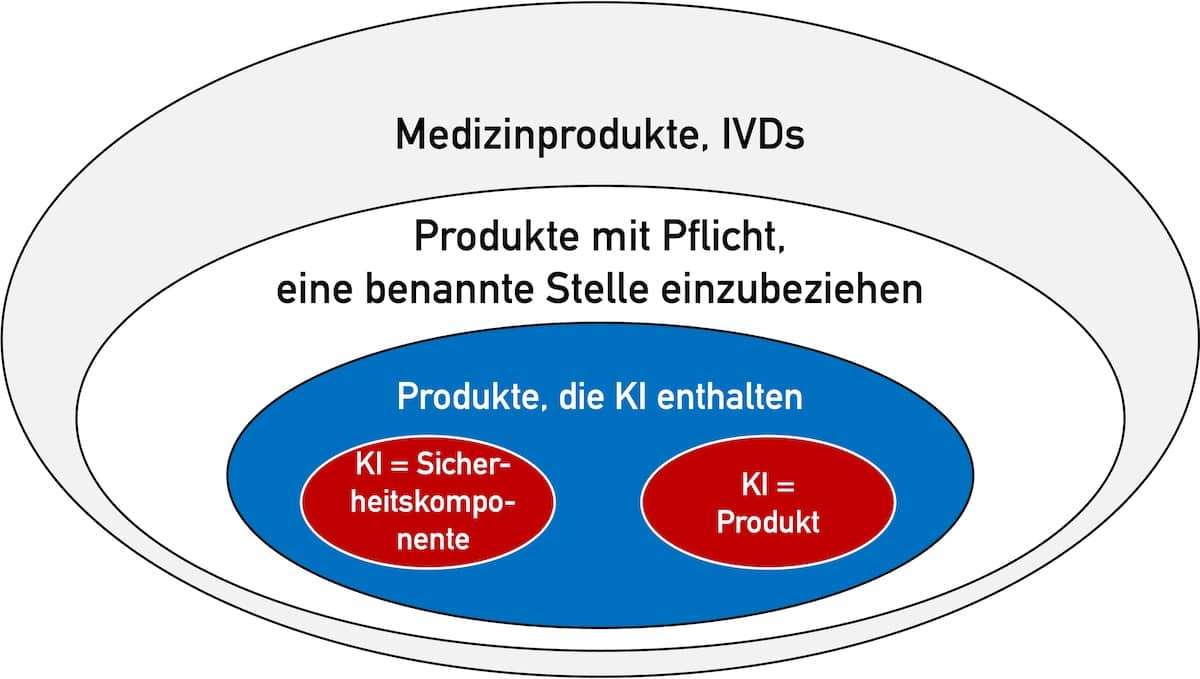
Die EU-KI-Verordnung (EU AI Act) ist veröffentlicht. Viele Hersteller von Medizinprodukten und IVD sowie andere Akteure im Gesundheitswesen stehen vor der großen Aufgabe, den über 140 Seiten umfassenden Gesetzestext zu verstehen und die Anforderungen zu erfüllen. Beachten Sie: Verstöße gegen den AI Act werden mit Geldstrafen in Höhe von bis zu 7 % des jährlichen Umsatzes…
Details
Medizinprodukteberater spielen eine zentrale Rolle, um die Sicherheit von Medizinprodukten zu gewährleisten. Die Position ist dem Pharmaberater (§ 75 AMG) nachgebildet. Die EU-Verordnungen MDR und IVDR kennen dieses Konzept nicht. Doch der Medizinprodukteberater ist im nationalen Recht verankert. Deutschland und Österreich fordern die Rolle des Medizinprodukteberaters im nationalen Recht (Medizinprodukterecht-Durchführungsgesetz (MPDG) in Deutschland und Medizinproduktegesetz…
Details
Krankenhausinformationssysteme (KIS) zählen zu den klinischen Informationssystemen. Als zentraler Teil der IT-Infrastruktur von Krankenhäusern dienen sie der digitalen Verwaltung und Verarbeitung sämtlicher administrativer und medizinischer Patientendaten in einem Krankenhaus. Ein KIS fungiert als elektronische Patientenakte und steuert Prozesse: von der Aufnahme über Diagnose und Behandlung bis zu Entlassung und Abrechnung. Dieser Artikel beleuchtet unter Berücksichtigung…
Details
Medizinprodukte der Klasse IIa gehören zu den häufigsten Produkten auf dem europäischen Markt. Dieser Artikel erklärt, welche Produkte in diese Klasse fallen, welche Klassifizierungsregeln relevant sind und welche regulatorischen Konsequenzen sich daraus ergeben.
Weil die Güte der Sterilisation von Medizinprodukten entscheidend für die Sicherheit dieser Medizinprodukte ist, sind die Auswahl und die Validierung des Sterilisationsverfahrens regelmäßig Gegenstand von Audits und Inspektionen. Dieser Artikel verschafft einen schnellen Überblick über die verschiedenen Sterilisationsverfahren sowie die regulatorischen Anforderungen bei Medizinprodukten und liefert Best Practices, um Prüfungen durch Behörden und Benannte Stellen…
Details
Die MDR enthält speziell für Software eine Klassifizierungsregel: Regel 11. Diese Regel 11 hat Sprengkraft! Sie hat das Potenzial, die Innovationskraft in Europa weiter zu schwächen. Hersteller sollten die Interpretation der MDCG kennen, um Fehlklassifizierungen von Software zu vermeiden und der Argumentation Benannter Stellen und Behörden folgen zu können. Diese Interpretation lernen Sie in diesem…
Details
Am 16.12.2025 hat die EU-Kommission ihren Vorschlag zur Überarbeitung von MDR und IVDR veröffentlicht, der bereits als MDR 2.0 bzw. IVDR 2.0 tituliert wird. Doch profitieren die Hersteller wirklich davon? Antworten gibt dieser Artikel.
Die EU plant, mit der neuen EU-Verordnung zu Batterien und Altbatterien („Batterieverordnung“) die bestehende Richtlinie 2006/66/EG zu ersetzen. Dieser Artikel klärt darüber auf,
Details
Müssen Medizinproduktehersteller eine KI wie ChatGPT validieren, die sie bei der Entwicklung, Produktion, Zulassung und Überwachung ihrer Produkte einsetzen? Falls ja, wie soll das gelingen mit Modellen, die nichtdeterministische Ergebnisse liefern? Antworten darauf und auf die Frage, was Ihre Auditoren erwarten (sollten), gibt dieser Fachartikel.
Details
Rechtliche Anforderungen und praktische Umsetzung nach MDR/IVDR EU-Bevollmächtigte unterliegen nicht nur den rechtlichen Vorgaben der MDR und IVDR. Sie haften auch für Verstöße gegen das Medizinprodukterecht. Dieser Fachartikel gibt praxisnahe Antworten auf alle regulatorischen Fragen zum EU-REP mit konkreten Handlungsempfehlungen vom führenden Beratungsunternehmen für Medizinprodukte-Regulierung. Er wendet sich an Non-EU-Medizinproduktehersteller sowie an Regulatory-Affairs-Manager, Qualitätsmanager, PRRCs…
Details