Wie Sie eine Benefit-Risk-Abwägung (Nutzen-Risiko-Abwägung) durchführen sollen, verrät die FDA in einem Guidance-Dokument. Es trägt den Titel “Factors to Consider When Making Benefit-Risk Determinations in Medical Device Premarket Approval and De Novo Classifications”, aktuell in der Ausgabe vom 30. August 2019.
Dieses Guidance-Dokument zur Benefit-Risk-Abwägung ist nicht nur bei FDA-Zulassungen sehr hilfreich. Nutzen Sie es auch bei der abschließenden Nutzen-Risiko-Bewertung gemäß ISO 14971.
Wie die „Benefit-Risk Guidance“ hilfreich sein kann – auch in Europa
Das Medizinprodukterecht gleicht sich in Europa und USA auch dahingehend, dass die zentrale Forderung lautet:
Das Gerät muss sicher sein. Etwaige Risiken müssen gemessen am Nutzen für den Patienten vertretbar sein.
Fast wörtlich formulieren das die MDR und der Food, Drug and Cosmetic Act (FD&C) in den USA.
Doch wie weist man nach, dass die Risiken mit dem Nutzen vereinbar sind? Bei der Beantwortung dieser Frage hilft dieses Dokument: Es zeigt, wie man eine Nutzen-Risiken-Bestimmung (benefit-risk determination) durchführt. Damit erhalten Sie die Basis, um eine Risikoakzeptanzmatrix zu erstellen.
Das Dokument enthält als Leitfaden ein Template, das wir Ihnen als Word-Datei hier zum Download bereitstellen.
Sie können sich hier das Template herunterladen.
Wann Sie die „Benefit-Risk Guidance“ beachten müssen
Laut FDA sollten Sie das Dokument immer dann beachten, wenn Sie eine „PMA-Zulassung“ (Pre Market Approval) oder gar einen „de novo classification request“ stellen. Für 510(k)-Zulassungen hingegen hat die FDA eine separate Leitlinie zu den Benefit-Risk Faktoren veröffentlicht. Gleiches gilt für IDEs (Investigational Device Exemptions), für welche die FDA ein eigenes Guidance-Dokument bereitstellt.
Man kann also etwas vereinfachend sagen: Immer, wenn Sie ein Produkt in den USA in den Markt bringen wollen – es sei denn, es ist von der Zulassung befreit –, sollten Sie das jeweilige „Benefit-Risk Guidance“-Document nicht nur lesen, sondern auch dessen Vorgaben erfüllen.
Was die „Benefit-Risk Guidance“ der FDA besagt
Aufbau des Dokuments
Das Dokument ist in fünf Kapitel gegliedert.
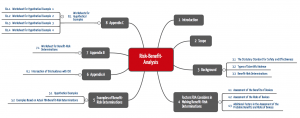
Übersicht über die Kapitel
- Introduction: Die FDA äußert sich, wie verbindlich Sie das Dokument verstanden haben will.
- Scope: Das Dokument ist im Wesentlichen bei allen Einreichungen und Klassifizierungsanfragen zu berücksichtigen.
- Background: Die FDA betont, wie wichtig der wissenschaftliche (d. h. systematische und objektive) Nachweis sowohl des Nutzens als auch der Risiken ist. (Dazu später mehr.)
- Factors: Das ist der eigentliche Inhalt. Die FDA legt dar, welche Faktoren bei der Nutzen-Risiko-Analyse zu beachten sind. (Das übernächste Teilkapitel stellt Ihnen diese Faktoren vor.)
- Examples: Konkrete (aber erfundene) Beispiele zeigen auf, wie die FDA für Produkte das Nutzen-Risiko-Verhältnis bestimmen und bewerten würde.
Wissenschaftliche Evidenz
Der Nachweis der Sicherheit und des Nutzens kann oft über klinische und nicht-klinische Daten erbracht werden.
Klinische Daten
- Klinische Studien
- Fallstudien
- Erfahrung
- Experimente an Leichen, Gewebe
Nicht-klinische Daten
- Tests, z. B. Leistungsfähigkeit inkl.
- Biokompatibilität, Toxizität, Sterilität
- Mechanische Stabilität
- Elektrische Sicherheit und elektromagnetische Verträglichkeit
- Software-Tests
- Usability Validierung
- Tierversuche, Zellexperimente
- Computer-Simulationen
Allerdings geben diese Daten alleine keine ausreichende Auskunft über das Nutzen-Risiko-Verhältnis.
Faktoren: Die wesentliche Forderungen
Die FDA unterbreitet konkrete Vorschläge, welche Faktoren man bei der Nutzen-Risiken-Abwägung beachten sollte. Interessanterweise sind das nicht nur die Nutzen und Risiken.
Beispielsweise sollen auch Präferenzen der Patienten, die Verfügbarkeit von Alternativen oder die Zuverlässigkeit der Daten einbezogen werden.
Die FDA geht in Kapitel 4 ihres Guidance-Dokuments auf jeden dieser Faktoren ein. Sie begründet jeden Faktor und nennt Kriterien für dessen Bewertung. Diese finden sich dann auch im „Worksheet“, dem Template, das Sie sich hier herunterladen können.
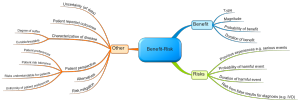
Bewertung des FDA-Dokuments
Das Dokument zeichnet sich aus durch:
- Konkrete Anregungen, welche Faktoren bei einer Nutzen-Risiko-Analyse zu beachten sind – neben dem Nutzen und den Risiken
- Viele Beispiele
- Humor (Kannten Sie schon das Produkt, mit dem man alle Erinnerung abspeichern und dafür das Gehirn entfernen kann?)
- Hilfreiches Template
Weitere Leitlinie zur Benefit-Risk-Abschätzung
Die FDA hat am 27.12.2016 ein weiteres Guidance-Dokument mit dem Titel „Factors to Consider Regarding Benefit-Risk in Medical Device Product Availability, Compliance, and Enforcement Decisions“ veröffentlicht. Wir werden es Ihnen in einem weiteren Beitrag vorstellen.
Änderungshistorie
- 2024-10-16: Aktualisiert auf die aktuelle Guidance von 2019
- Referenzen zu den weiteren Benefit-Risk-Guidances ergänzt