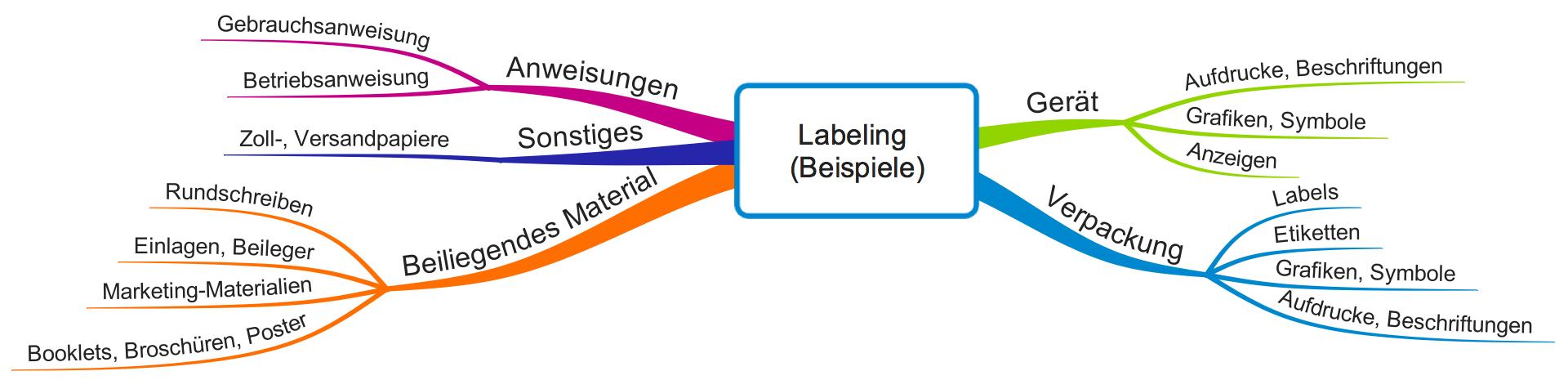
Elektronische Gebrauchsanweisung für Medizinprodukte
Die EU-Verordnung 2017/745 (MDR) legt die allgemeinen Anforderungen an die Gebrauchsanweisung (instructions for use, kurz IFU) fest. Ob sie auch in elektronischer Form vorliegen darf (eIFU), regelt die Durchführungsverordnung (EU) 2021/2226. Diese wurde durch die Durchführungsverordnung (EU) 2025/1234 überarbeitet. Eine konsolidierte Version ist mittlerweile ebenfalls verfügbar. Wir haben die Voraussetzungen für die elektronische Gebrauchsanweisung für Sie…
Details