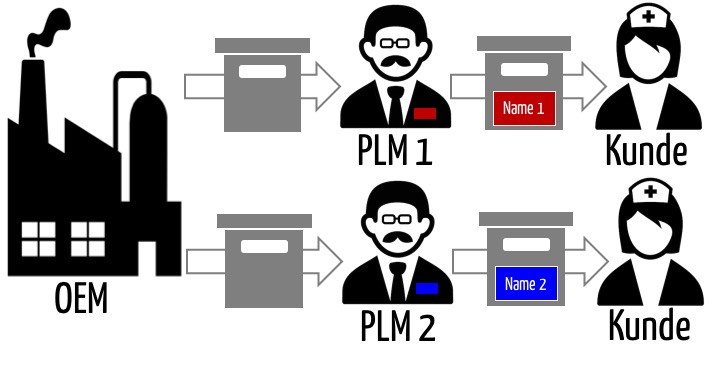
Die FDA Cybersecurity Guidance Documents
Die Cybersecurity von Medizinprodukten ist nicht nur ein Schwerpunkt der FDA, sondern auch anderer Gesetzgeber und Behörden, sowohl in den US als auch anderen Märkten. Das ist nachvollziehbar, Die USA hat den „Food, Drug & Cosmetic Act“ (FD&C) um Anforderungen an „Cyber Devices“ ergänzt, und die FDA mehrere Guidance Documents zur Cybersecurity veröffentlicht, die dieser…
Details