Medizinprodukte der Klasse IIa gehören zu den häufigsten Produkten auf dem europäischen Markt. Dieser Artikel erklärt, welche Produkte in diese Klasse fallen, welche Klassifizierungsregeln relevant sind und welche regulatorischen Konsequenzen sich daraus ergeben.
- Die MDR weist die Klasse IIa Medizinprodukten mit mittlerem Risiko zu.
- Diese Klassifizierung hat wenig Einfluss auf die gesetzlichen Anforderungen an das Medizinprodukt.
- Die Klassifizierung wirkt sich allerdings auf das Konformitätsbewertungsverfahren und die Intensität der Überwachung durch Benannte Stellen aus.
1. Definition: Was ist ein Medizinprodukt der Klasse IIa?
Medizinprodukte der Klasse IIa sind Produkte mit mittlerem Risikopotenzial nach der EU-Medizinprodukteverordnung (MDR) 2017/745. Sie erfordern die Einbindung einer Benannten Stelle im Konformitätsbewertungsverfahren. Typische Vertreter sind diagnostische Geräte, kurzfristig invasive Produkte oder aktive therapeutische Produkte zur Energieabgabe, sofern diese Energie keine potenzielle Gefährdung darstellt.
Einordnung im Klassifizierungssystem
Die MDR unterscheidet vier Risikoklassen:
| Klasse | Risikopotenzial | Beispiele |
|---|---|---|
| I | Niedrig | Verbandmull, Gehstützen |
| IIa | Mittel | Blutdruckmessgeräte, Einmalkatheter |
| IIb | Erhöht | Beatmungsgeräte, Röntgengeräte |
| III | Hoch | Herzschrittmacher, Hüftimplantate |
Wichtig: Die Klassifizierung ergibt sich aus der Zweckbestimmung des Herstellers – nicht aus der technischen Komplexität oder dem Preis.
2. Beispiele: Welche Produkte gehören zur Klasse IIa?
Typische Klasse-IIa-Produkte nach Kategorie
| Kategorie | Beispiele |
|---|---|
| Diagnostische Geräte | Blutdruckmessgeräte, Fieberthermometer |
| Kurzfristig invasive Produkte | Einmalkatheter (< 60 Min.), Kanülen, Trachealtuben |
| Aktive therapeutische Geräte | TENS-Geräte, Ultraschall-Therapiegeräte |
| Kontaktlinsen | Tageslinsen, weiche Kontaktlinsen (nicht Langzeit) |
| Wundversorgung | Wundauflagen (nicht resorbierbar, nicht für chronische Wunden) |
| Software | DiGA zur Therapieunterstützung (ohne Diagnose schwerer Erkrankungen) |
Die gleiche Produktkategorie kann je nach Zweckbestimmung unterschiedlich klassifiziert werden.
Beispiel Kontaktlinsen:
- Tageslinsen → Klasse IIa
- Langzeit-Kontaktlinsen (> 30 Tage) → Klasse IIb
3. Klassifizierungsregeln: Welche Regeln führen zu Klasse IIa?
Die Klassifizierung erfolgt nach Anhang VIII der MDR. Folgende Regeln können zu Klasse IIa führen:
Übersicht relevanter Regeln
| Regel | Produkttyp | Klasse IIa, wenn… |
|---|---|---|
| 5 | Nicht-invasiv | zur Aufbewahrung/Leitung von Blut, Körperflüssigkeiten oder Gewebe bestimmt |
| 6 | Nicht-invasiv | zur Veränderung der Zusammensetzung von Blut/Körperflüssigkeiten durch Filtration, Zentrifugation oder Gas-/Wärmeaustausch bestimmt |
| 7 | Invasiv (Körperöffnungen) | zur kurzfristigen Anwendung (< 60 Min.) bestimmt ODER langfristig in Mundhöhle/Gehörgang/Nasenhöhle |
| 9 | Aktiv therapeutisch | Energieabgabe auf nicht potenziell gefährliche Weise erfolgt |
| 10 | Aktiv diagnostisch | zur direkten Diagnose/Überwachung vitaler Körperfunktionen (ohne unmittelbare Gefahr) bestimmt |
| 11 | Software | Information für Therapieentscheidungen, wenn Fehler keine schwere Verschlechterung verursacht |
| 12 | Arzneimittelverabreichung | Verabreichung erfolgt auf nicht potenziell gefährliche Weise |
Die Einstufung hängt vom jeweiligen Fall ab. Beispielsweise ist ein Verbandmull in Kontakt mit verletzter Haut höher klassifiziert, Katheter gibt es verschiedene, ein ZVK ist ein Klasse III Produkt.
Besonderheit: Regel 11 (Software als Medizinprodukt)
Software wird nach Regel 11 klassifiziert. Die Einstufung hängt ab von
- der Art der bereitgestellten Information,
- Entscheidungen, die darauf basieren, sowie
- Konsequenzen einer Fehlinformation.
Regel 11 im Detail: Die Klassifizierung von Software ist komplex und wird durch die geplante MDR-Revision voraussichtlich angepasst.
→ Eine ausführliche Darstellung finden Sie im Fachartikel Regel 11 – Software als Medizinprodukt.
4. Entscheidungsbaum: Ist mein Produkt Klasse IIa?
Der folgende Entscheidungsbaum führt durch die wichtigsten Klassifizierungspfade:
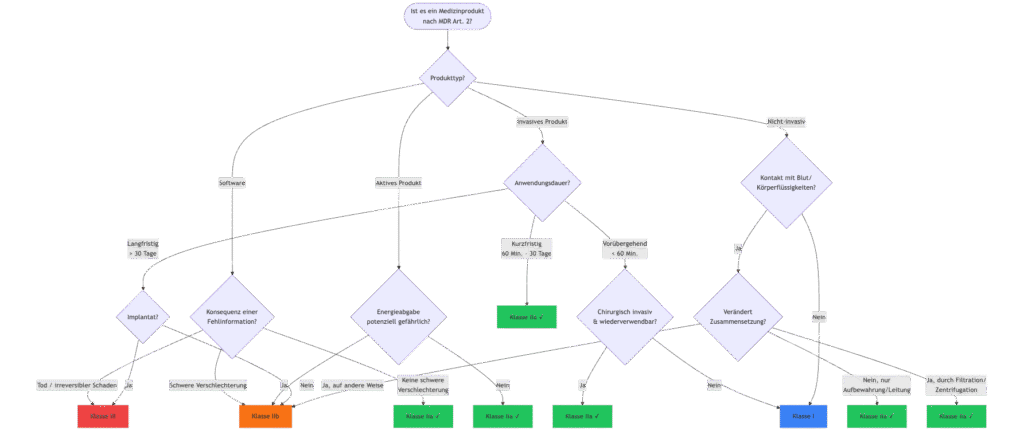
Dieser Entscheidungsbaum deckt die häufigsten Fälle ab. Er bildet aber nicht alle 22 Klassifizierungsregeln vollständig ab. Im Zweifel ist eine detaillierte Prüfung anhand von Anhang VIII MDR erforderlich.
5. Konsequenzen: Was bedeutet Klasse IIa konkret?
Die Klassifizierung hat direkte Auswirkungen auf den regulatorischen Aufwand:
a. Anforderungen im „Klassenvergleich“
| Aspekt | Klasse I | Klasse IIa | Klasse IIb | Klasse III |
|---|---|---|---|---|
| Benannte Stelle erforderlich | Nein* | Ja | Ja | Ja |
| Konformitäts-bewertung | Anhang IV | Anhang IX (Kap. I+III) oder XI Abschnitt 10 oder Abschnitt 18 | Anhang IX (Kap. I+III) oder X+XI | Anhang IX oder X+XI Teil A |
| TD-Prüfung durch Benannte Stelle | Nein | Stichprobenbasiert | Stichprobenbasiert | Vollständig |
| PSUR-Frequenz | Nicht erforderlich | Mind. alle 2 Jahre | Mind. jährlich | Mind. jährlich |
| Klinische Prüfung | Selten | Meist nein | Häufiger | Oft erforderlich |
| Expert Panel | Nein | Nein | Nur implantierbar | Ja (neue Produkte) |
| Gebrauchs-anweisung | Kann entfallen** | Kann entfallen** | Immer erforderlich | Immer erforderlich |
| PRRC erforderlich | Ja | Ja | Ja | Ja |
| UDI-Pflicht | Ja | Ja | Ja | Ja |
| EUDAMED-Registrierung | Ja | Ja | Ja | Ja |
*Ausnahme: Klasse Is, Im, Ir erfordern eine Benannte Stelle
**Wenn sichere Anwendung ohne Gebrauchsanweisung gewährleistet (Anhang I, Abschnitt 23.1)
b. Konformitätsbewertungsverfahren für Klasse IIa
Für Klasse IIa stehen zwei Wege offen:
- Anhang IX, Kapitel I + III: QMS-Bewertung + TD-Prüfung auf Stichprobenbasis
- Anhang XI, Abschnitt 10 oder Abschnitt 18: Produktprüfung
Details zu den Konformitätsbewertungsverfahren erhalten Sie in unserem Fachartikel zur Konformitätsbewertung nach MDR.
c. Stichprobenprüfung der Technischen Dokumentation (Sampling)
Bei Klasse IIa prüft die Benannte Stelle nicht jede Technische Dokumentation vollständig. Stattdessen erfolgt eine risikobasierte Stichprobenauswahl:
Auswahlkriterien:
- Produktkategorien (Generic Device Groups)
- Mindestens ein Produkt pro Kategorie
- Neue Produkte werden priorisiert
- Produkte mit Vorkommnissen werden priorisiert
- Stichprobengröße steigt mit Portfoliogröße
Überwachungsaudits: Bei jährlichen Audits werden weitere Stichproben geprüft.
Auch wenn Ihre TD nicht geprüft wird, muss sie vollständig und konform sein. Die Benannte Stelle kann jederzeit zusätzliche Prüfungen durchführen.
d. PSUR: Periodic Safety Update Report
Hersteller von Klasse-IIa-Produkten müssen einen PSUR erstellen.
- Frequenz: Mindestens alle 2 Jahre (bei Klasse IIb/III: jährlich)
- Inhalt: Zusammenfassung aller PMS-Daten, Nutzen-Risiko-Bewertung
- Vorlage: bei der Benannten Stelle
Details zum PSUR entnehmen Sie unserem Fachartikel zu Post-Market Surveillance und PSUR.
6. Worauf hat die Klassifizierung keinen Einfluss?
Viele Anforderungen gelten klassenunabhängig:
| Anforderung | Gilt für alle Klassen? |
|---|---|
| Grundlegende Sicherheits- und Leistungsanforderungen (Anhang I) | ✓ Ja |
| Risikomanagement nach ISO 14971 | ✓ Ja |
| Qualitätsmanagementsystem | ✓ Ja |
| Post-Market Surveillance (Grundpflicht) | ✓ Ja |
| Technische Dokumentation (Struktur nach Anhang II/III) | ✓ Ja |
| Vigilanz-Meldepflichten | ✓ Ja |
| Produkthaftung | ✓ Ja |
Die Klassifizierung bestimmt primär den Umfang der externen Prüfung durch die Benannte Stelle – nicht den internen Qualitätsaufwand. Auch Klasse-I-Produkte erfordern ein vollständiges QMS und eine konforme Technische Dokumentation.
7. Internationale Perspektive
Gilt Klasse IIa auch außerhalb der EU?
Nein. Die MDR-Klassifizierung gilt nur im Europäischen Wirtschaftsraum (EU + Island, Liechtenstein, Norwegen) sowie in der Schweiz.
Andere Märkte haben eigene Systeme:
| Markt | System | Vergleichbarkeit |
|---|---|---|
| USA (FDA) | Class I, II, III | Nicht direkt vergleichbar |
| China (NMPA) | Class I, II, III | Eigene Regeln |
| Japan (PMDA) | Class I–IV | Vier Klassen |
Beispiel: Ein Klasse-IIa-Produkt in der EU kann in den USA Class II oder Class III sein.
→ Für internationale Zulassungsstrategien: Beratung zur regulatorischen Strategie
8. Übergangsfristen: Was gilt für Bestandsprodukte?
Einige Produkte werden durch die MDR höher klassifiziert als durch die vorangegangene MDD:
Beispiele für Hochstufungen:
- Wiederverwendbare chirurgische Instrumente: I → Ir (mit Benannter Stelle)
- Bestimmte Software: I → IIa oder höher
- Zentralvenöse Katheter zur kurzzeitigen Anwendung: IIa III
Details zu Übergangsfristen und Legacy Devices gibt dieser Fachartikel zu den MDR-Übergangsfristen.
9. Kann man die Klassifizierung beeinflussen?
Die Klassifizierung ergibt sich aus der Zweckbestimmung – diese legt der Hersteller fest.
Legitime Strategien
| Strategie | Beispiel |
|---|---|
| Funktionsumfang begrenzen | Software zeigt nur anstatt zu analysieren → niedrigere Klasse |
| Anwendungsdauer begrenzen | Kurzfristig statt langfristig invasiv → niedrigere Klasse |
| Indikation präzisieren | Ausschluss bestimmter Patientengruppen |
| Produktaufteilung | Trennung in mehrere Produkte mit unterschiedlichen Klassen |
- Regulatorische Probleme (Audits, Marktüberwachung)
- Haftungsrisiken
- Reputationsschäden
10. Zusammenfassung
Medizinprodukte der Klasse IIa:
- Es handelt sich um Produkte mit mittlerem Risikopotenzial.
- Es ist die Einbeziehung einer Benannten Stelle erforderlich.
- Die Prüfung der Technischen Dokumentation erfolgt auf Stichprobenbasis.
- Ein PSUR muss mind. alle 2 Jahre erstellt werden.
- Die Erstellung einer Gebrauchsanweisung kann unter Umständen entfallen.
Wichtigste Klassifizierungsregeln: 5, 6, 7, 9, 10, 11, 12
Entscheidend: Die Zweckbestimmung bestimmt die Klasse – nicht die Technik.
Sind Sie unsicher bei der Klassifizierung Ihres Produkts? In unserer Beratung „Regulatorische Strategie“ unterstützen wir Sie bei:
- Klassifizierung nach MDR (und international)
- Qualifizierung als Medizinprodukt vs. Nicht-Medizinprodukt
- Optimierung der Zweckbestimmung
- Entwicklung einer globalen Zulassungsstrategie


