Der Bereich „Regulatory Affairs“ umfasst über 200 Aufgaben, die bei der Entwicklung und Zulassung von Medizinprodukten zu erledigen sind.
Sie finden hier eine Übersicht über die wichtigsten Inhalte, damit Sie Ihr Produkt schnell zulassen können.
Inhalt
Sie finden auf dieser Seite Fachartikel zu diesen Themen:
- Was Regulatory Affairs ist
- Regulatorische Anforderungen
- Zulassung und Dokumentation
- Behörden, Institutionen und Verbänden
- Weitere Themen der Regulatory Affairs
1. Was Regulatory Affairs ist
Regulatory Affairs umfasst die Prozesse und Aktivitäten, die sicherstellen, dass Medizinprodukte die regulatorischen Anforderungen der Länder erfüllen, in denen sie verkauft werden sollen. Dazu gehören die
- Einholung der erforderlichen Genehmigungen und Freigaben von den Aufsichtsbehörden,
- Einhaltung der geltenden Vorschriften und Normen sowie
- Aufrechterhaltung der Konformität während des gesamten Produktlebenszyklus bis zur Außerbetriebnahme.
Zu den Aufgaben des Bereichs Regulatory Affairs gehört auch die Überwachung von Änderungen der Vorschriften und Normen und die Kommunikation dieser Änderungen mit den Interessengruppen innerhalb des Unternehmens, um eine kontinuierliche Einhaltung zu gewährleisten.
Damit spielt Regulatory Affairs eine entscheidende Rolle, wenn es darum geht, sicherzustellen, dass Medizinprodukte sicher und wirksam sind und den gesetzlichen Anforderungen entsprechen.
2. Regulatorische Anforderungen
a) Deutschland
b) Europa
c) USA
d) Andere Märkte
3. Zulassung und Dokumentation
a) Zulassung
Finden Sie weitere Informationen zur internationalen Zulassung.
b) Qualifizierung und Klassifizierungen (Wie ist mein Produkt einzuteilen?)
c) Technische Dokumentation (Was muss ich pro Produkt dokumentieren?)
d) Qualitätsmanagement (Was sollte Ihre Firma erfüllen?)
Das Qualitätsmanagement zählt üblicherweise nicht zur Verantwortung von Regulatory Affairs. Dennoch listen wir Ihnen einige wichtige Artikel.
e) Regulatorische Rollen
Sie finden hier Fachartikel zu mehreren regulatorischen Rollen;
4. Behörden, Institutionen und Verbände
a) Deutschland
| BfArM: Bundesamt für Arzneimittel und Medizinprodukte |
| DIMDI (Deutsches Institut für medizinische Informatik; wurde inzwischen in das BfArM integriert) |
| DAkkS, die deutsche Akkreditierungsstelle |
| Länderbehörden: Regierungspräsidien, Gewerbeaufsichtsämter, Regierungen |
b) Europa
c) International
| IMDRF: International Medical Device Regulators Forum |
5. Regulatory Affairs: Weitere Themen
Die Aufgaben von Regulatory Affairs umfassen auch das Finden und Beseitigen von Abweichungen und Nicht-Konformitäten. Die (notfallmäßige) Beseitigung nennt sich Remediation.
Beachten Sie die Vor- und Nachteile von Regulatory Information Management Systemen (RIMS) und deren Rolle bei der digitalen Transformation der Hersteller.
Ein Teil der Aufgaben von Regulatory Affairs ist die Regulatory Intelligence.
Benötigen Sie Unterstützung?
Haben Sie noch Fragen, beispielsweise zur Zulassung Ihrer Produkte? Dann nutzen Sie das kostenfreie Micro-Consulting.
Falls Sie Unterstützung dabei wünschen, Ihre Medizinprodukte gesetzeskonform zu entwickeln und „zuzulassen“, dann nehmen Sie gleich Kontakt auf. Das Team das Johner Instituts hilft gerne!
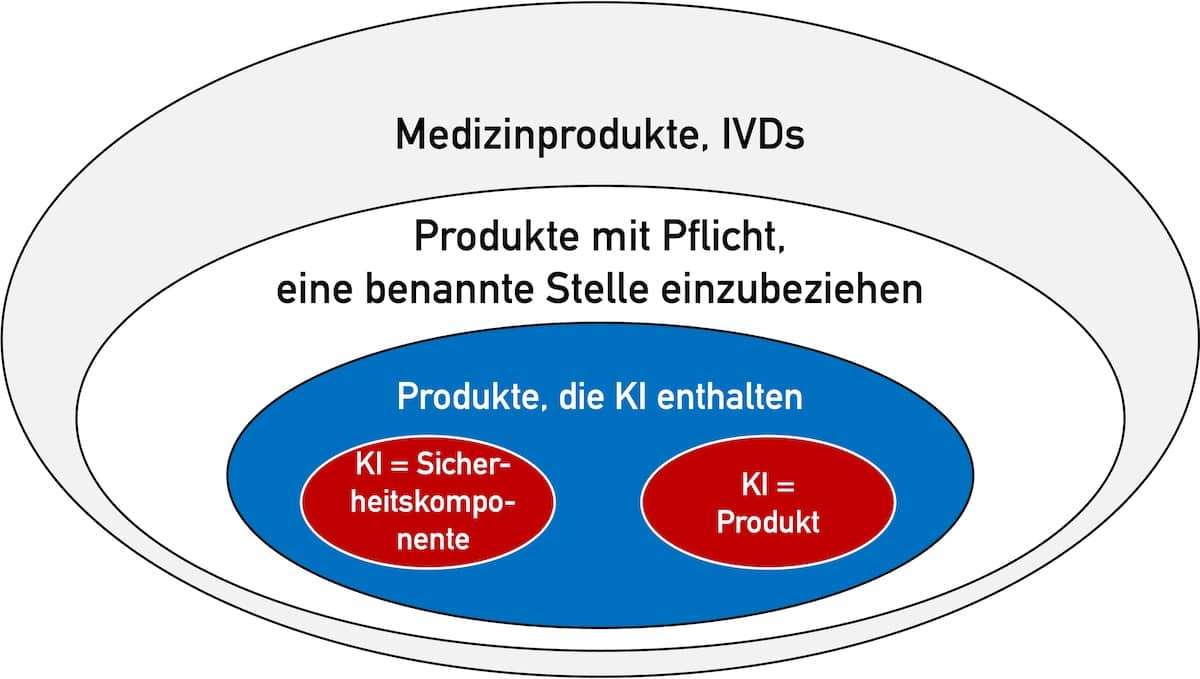
Die EU-KI-Verordnung (EU AI Act) ist veröffentlicht. Viele Hersteller von Medizinprodukten und IVD sowie andere Akteure im Gesundheitswesen stehen vor der großen Aufgabe, den über 140 Seiten umfassenden Gesetzestext zu verstehen und die Anforderungen zu erfüllen. Beachten Sie: Verstöße gegen den AI Act werden mit Geldstrafen in Höhe von bis zu 7 % des jährlichen Umsatzes…
Details
Medizinprodukte-Hersteller sind verpflichtet, klinische Daten vor und nach der Zulassung ihrer Produkte systematisch zu sammeln und auszuwerten. Die EU-Medizinprodukteverordnung MDR hat die Anforderungen an den Umfang und die Qualität dieser klinischen Daten erhöht. Dieser Artikel verschafft Ihnen einen Überblick über die regulatorischen Anforderungen und gibt Tipps, welche klinischen Daten Medizinproduktehersteller auf welche Weise sammeln und…
Details
Medizinprodukteberater spielen eine zentrale Rolle, um die Sicherheit von Medizinprodukten zu gewährleisten. Die Position ist dem Pharmaberater (§ 75 AMG) nachgebildet. Die EU-Verordnungen MDR und IVDR kennen dieses Konzept nicht. Doch der Medizinprodukteberater ist im nationalen Recht verankert. Deutschland und Österreich fordern die Rolle des Medizinprodukteberaters im nationalen Recht (Medizinprodukterecht-Durchführungsgesetz (MPDG) in Deutschland und Medizinproduktegesetz…
Details
Krankenhausinformationssysteme (KIS) zählen zu den klinischen Informationssystemen. Als zentraler Teil der IT-Infrastruktur von Krankenhäusern dienen sie der digitalen Verwaltung und Verarbeitung sämtlicher administrativer und medizinischer Patientendaten in einem Krankenhaus. Ein KIS fungiert als elektronische Patientenakte und steuert Prozesse: von der Aufnahme über Diagnose und Behandlung bis zu Entlassung und Abrechnung. Dieser Artikel beleuchtet unter Berücksichtigung…
Details
Decision Support Systems, zu Deutsch Entscheidungsunterstützungssysteme, finden auch in der Medizin zunehmend Anwendung. Handelt es sich dabei um Medizinprodukte, müssen diese die gesetzlichen Anforderungen (z. B. die grundlegenden Anforderungen) erfüllen. Der Hype um die künstliche Intelligenz, insbesondere das Machine Learning, und Anwendungen wie Watson wecken Hoffnungen an die Leistungsfähigkeit von Decision Support Systemen. Dieser Artikel stellt…
Details
Medizinprodukte der Klasse IIa gehören zu den häufigsten Produkten auf dem europäischen Markt. Dieser Artikel erklärt, welche Produkte in diese Klasse fallen, welche Klassifizierungsregeln relevant sind und welche regulatorischen Konsequenzen sich daraus ergeben.
Weil die Güte der Sterilisation von Medizinprodukten entscheidend für die Sicherheit dieser Medizinprodukte ist, sind die Auswahl und die Validierung des Sterilisationsverfahrens regelmäßig Gegenstand von Audits und Inspektionen. Dieser Artikel verschafft einen schnellen Überblick über die verschiedenen Sterilisationsverfahren sowie die regulatorischen Anforderungen bei Medizinprodukten und liefert Best Practices, um Prüfungen durch Behörden und Benannte Stellen…
Details
Hersteller, die Machine Learning (ML) in ihren Medizinprodukten oder IVD verwenden, müssen viele regulatorische Anforderungen erfüllen. Dieser Artikel gibt eine Übersicht über die wichtigsten Regularien und Best Practices für die Umsetzung. Er erspart Ihnen somit das Recherchieren und Lesen von hunderten Seiten und hilft Ihnen, sich perfekt auf das nächste Audit vorzubereiten.
Details
Die MDR enthält speziell für Software eine Klassifizierungsregel: Regel 11. Diese Regel 11 hat Sprengkraft! Sie hat das Potenzial, die Innovationskraft in Europa weiter zu schwächen. Hersteller sollten die Interpretation der MDCG kennen, um Fehlklassifizierungen von Software zu vermeiden und der Argumentation Benannter Stellen und Behörden folgen zu können. Diese Interpretation lernen Sie in diesem…
Details
Unter Software als Medizinprodukt (Software as Medical Device, SaMD) versteht man (eigenständige) Standalone-Software, die ein Medizinprodukt ist, aber nicht Teil eines solchen. Sie ist nicht zu verwechseln mit Medical Device Software im Sinne der EU. Wann müssen Sie als Hersteller Software als Medizinprodukt und wann als Medical Device Software qualifizieren? Das erfahren Sie hier – und können…
Details