Der Bereich „Regulatory Affairs“ umfasst über 200 Aufgaben, die bei der Entwicklung und Zulassung von Medizinprodukten zu erledigen sind.
Sie finden hier eine Übersicht über die wichtigsten Inhalte, damit Sie Ihr Produkt schnell zulassen können.
Inhalt
Sie finden auf dieser Seite Fachartikel zu diesen Themen:
- Was Regulatory Affairs ist
- Regulatorische Anforderungen
- Zulassung und Dokumentation
- Behörden, Institutionen und Verbänden
- Weitere Themen der Regulatory Affairs
1. Was Regulatory Affairs ist
Regulatory Affairs umfasst die Prozesse und Aktivitäten, die sicherstellen, dass Medizinprodukte die regulatorischen Anforderungen der Länder erfüllen, in denen sie verkauft werden sollen. Dazu gehören die
- Einholung der erforderlichen Genehmigungen und Freigaben von den Aufsichtsbehörden,
- Einhaltung der geltenden Vorschriften und Normen sowie
- Aufrechterhaltung der Konformität während des gesamten Produktlebenszyklus bis zur Außerbetriebnahme.
Zu den Aufgaben des Bereichs Regulatory Affairs gehört auch die Überwachung von Änderungen der Vorschriften und Normen und die Kommunikation dieser Änderungen mit den Interessengruppen innerhalb des Unternehmens, um eine kontinuierliche Einhaltung zu gewährleisten.
Damit spielt Regulatory Affairs eine entscheidende Rolle, wenn es darum geht, sicherzustellen, dass Medizinprodukte sicher und wirksam sind und den gesetzlichen Anforderungen entsprechen.
2. Regulatorische Anforderungen
a) Deutschland
b) Europa
c) USA
d) Andere Märkte
3. Zulassung und Dokumentation
a) Zulassung
Finden Sie weitere Informationen zur internationalen Zulassung.
b) Qualifizierung und Klassifizierungen (Wie ist mein Produkt einzuteilen?)
c) Technische Dokumentation (Was muss ich pro Produkt dokumentieren?)
d) Qualitätsmanagement (Was sollte Ihre Firma erfüllen?)
Das Qualitätsmanagement zählt üblicherweise nicht zur Verantwortung von Regulatory Affairs. Dennoch listen wir Ihnen einige wichtige Artikel.
e) Regulatorische Rollen
Sie finden hier Fachartikel zu mehreren regulatorischen Rollen;
4. Behörden, Institutionen und Verbände
a) Deutschland
| BfArM: Bundesamt für Arzneimittel und Medizinprodukte |
| DIMDI (Deutsches Institut für medizinische Informatik; wurde inzwischen in das BfArM integriert) |
| DAkkS, die deutsche Akkreditierungsstelle |
| Länderbehörden: Regierungspräsidien, Gewerbeaufsichtsämter, Regierungen |
b) Europa
c) International
| IMDRF: International Medical Device Regulators Forum |
5. Regulatory Affairs: Weitere Themen
Die Aufgaben von Regulatory Affairs umfassen auch das Finden und Beseitigen von Abweichungen und Nicht-Konformitäten. Die (notfallmäßige) Beseitigung nennt sich Remediation.
Beachten Sie die Vor- und Nachteile von Regulatory Information Management Systemen (RIMS) und deren Rolle bei der digitalen Transformation der Hersteller.
Ein Teil der Aufgaben von Regulatory Affairs ist die Regulatory Intelligence.
Benötigen Sie Unterstützung?
Haben Sie noch Fragen, beispielsweise zur Zulassung Ihrer Produkte? Dann nutzen Sie das kostenfreie Micro-Consulting.
Falls Sie Unterstützung dabei wünschen, Ihre Medizinprodukte gesetzeskonform zu entwickeln und „zuzulassen“, dann nehmen Sie gleich Kontakt auf. Das Team das Johner Instituts hilft gerne!
Mit der Verordnung 2021/2282 hat die EU ein Instrument geschaffen, um die Bewertung von Gesundheitstechnologien (Health Technology Assessment, HTA) unionsübergreifend zu vereinheitlichen. Dies soll es den Mitgliedstaaten leichter machen, über die gesundheitspolitischen Konsequenzen neuer Gesundheitstechnologien und deren Preisgestaltung zu entscheiden. Für Hersteller bzw. Entwickler entfällt im Idealfall doppelter Aufwand. Doch der Unionsgesetzgeber ist mit der…
Details
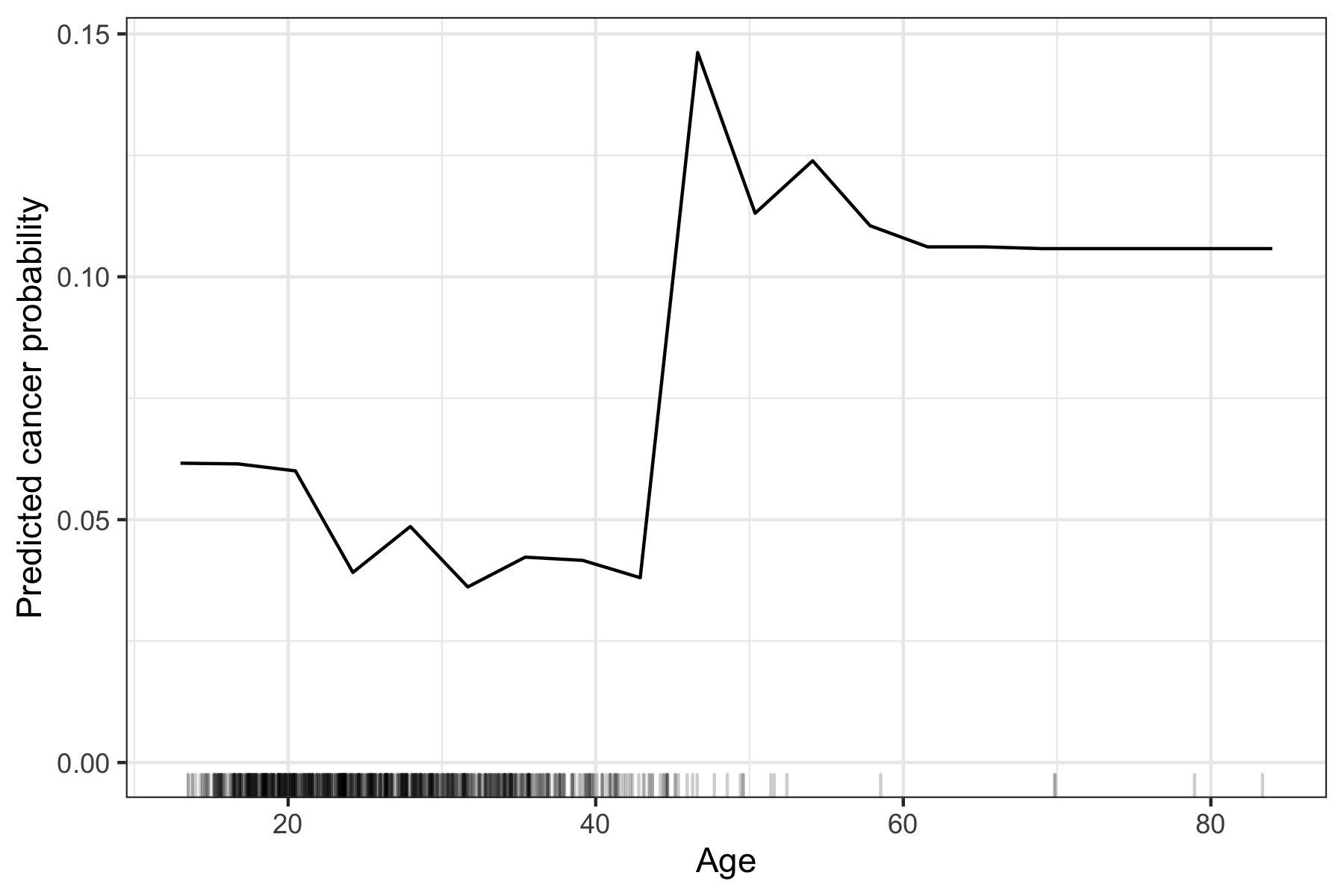
Mit einem Zytotoxizitätstest lässt sich eine Probe daraufhin überprüfen, wie stark diese die menschlichen Zellen schädigen oder sogar den Tod dieser Zellen verursachen kann. Normen und Gesetze verlangen von den Herstellern nachzuweisen, dass ihre Produkte nicht zytotoxisch sind. Mit einem guten Testaufbau gelingt der Nachweis, ob eine Probe 100 % zytotoxisch, d.h. stark zytotoxisch ist,…
Details
510(k)-Verfahren, auch “Premarket Notification” genannt, gehören zu den gängigsten Verfahren, nach denen in den USA Medizinprodukte zugelassen werden. Das Konzept basiert darauf, die Äquivalenz mit einem Vergleichsprodukt nachzuweisen. Doch dabei passieren schnell die immer gleichen Fehler, an denen die gesamte 510(k)-Zulassung scheitern kann. Das muss nicht sein! Erfahren Sie in diesem Beitrag, welches die fünf…
Details
Das Thema Nachhaltigkeit ist allgegenwärtig. In der Medizintechnik scheint sich der Trend aber langsamer durchzusetzen als in anderen Branchen. Kein Wunder, immerhin müssen Medizinprodukte eine Vielzahl an Anforderungen erfüllen, bevor sie auf den Markt dürfen. Doch stehen diese Anforderungen wirklich der Nachhaltigkeit im Wege? Dieser Beitrag zeigt auf, was es für Hersteller von Medizinprodukten zu…
Details
Wie wichtig gute Definitionen sind, stellt man z. B. fest, wenn es mit einem Gesprächspartner Missverständnisse gibt. Im schlimmeren Fall einer juristischen Auseinandersetzung entscheiden Definitionen darüber, ob ein Haftungsfall vorliegt oder sogar eine Straftat. Unklare Definitionen, insbesondere in Gesetzestexten, erhöhen die rechtliche Unsicherheit. Dieser Artikel zeigt einen Weg auf, wie Sie gute Definitionen schreiben und…
Details
Dass künstliche Intelligenz (KI oder AI) ein enormes Potenzial für die Medizin birgt, haben viele Hersteller bereits erkannt. Was aber, wenn die Schlüsse der KI für den Menschen nicht mehr nachvollziehbar sind? Ein reales und akutes Problem, bei dem das Konzept der “Interpretierbarkeit von KI” hilft. Die Interpretierbarkeit von maschinellem Lernen sorgt dafür, dass KI-basierte…
Details
Unter Post-Market Surveillance (Überwachung nach der Inverkehrbringung) versteht man einen proaktiven und systematischen Prozess, um aus Informationen über Medizinprodukte, die bereits in Verkehr gebracht wurden, notwendige Korrektur- und Vorbeugemaßnahmen (CAPA, corrective and preventive action) abzuleiten. Wir haben für Sie eine Checkliste zur Post-Market-Surveillance erstellt. Mit dieser Checkliste können Sie herausfinden, ob Sie die regulatorischen Anforderungen…
Details
Hersteller von Bestandsprodukten (legacy devices) können derzeit ihre Produkte noch auf dem Markt behalten, ohne einen Konformitätsnachweis nach der Verordnung 2017/745 über Medizinprodukte (MDR) zu erbringen. Spätestens mit Ende der Übergangsfrist müssen Hersteller jedoch die hierfür notwendigen klinischen Daten bereitstellen. Die Anforderungen an klinische Daten, die als Nachweis für die Konformität nutzbar sind, sind allerdings…
Details
Seit einigen Jahren geht die Harmonisierung von Normen in der EU nur schleppend voran. Das bekommen Hersteller von Medizinprodukten derzeit vor allem im Rahmen der EU-Verordnung zu Medizinprodukten (Medical Device Regulation, MDR, (EU) 2017/745) zu spüren. Diese löste zwar 2021 die Richtlinie 93/42/EWG über Medizinprodukte (Medical Device Directive, MDD) ab. Doch zur Verordnung harmonisierte Normen…
Details
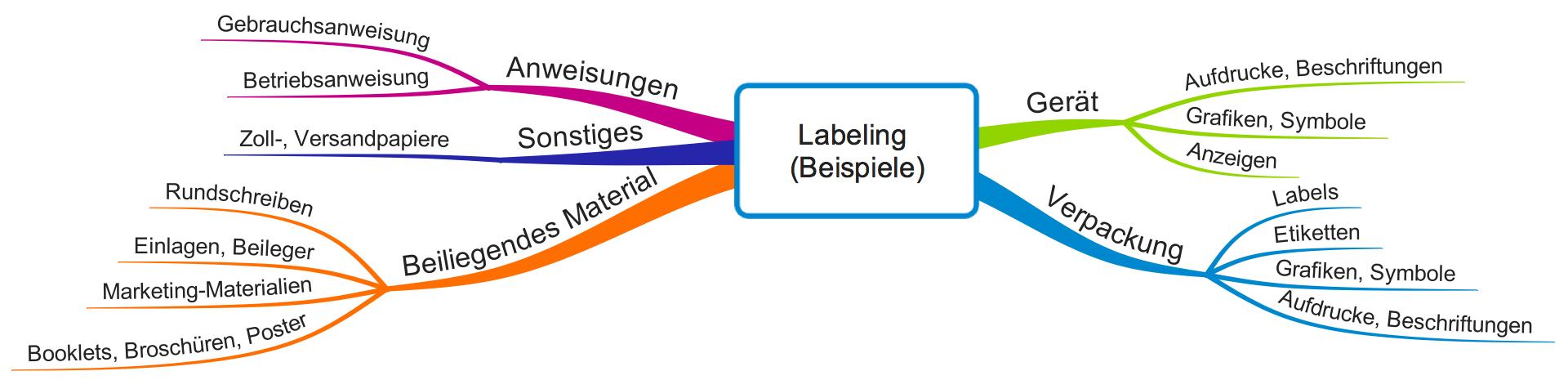
An das Labeling stellen sowohl die europäischen als auch die US-amerikanischen Regularien Anforderungen. Allerdings verstehen beide Rechtssysteme den Begriff nicht völlig identisch. Selbst die Schreibweisen unterscheiden sich: Labeling in den USA, Labelling in Europa. Erfahren Sie in diesem Artikel, was Sie beim Labeling jeweils beachten müssen. Apropos Schreibeweise: Wir verwenden in diesem Artikel das amerikanische…
Details