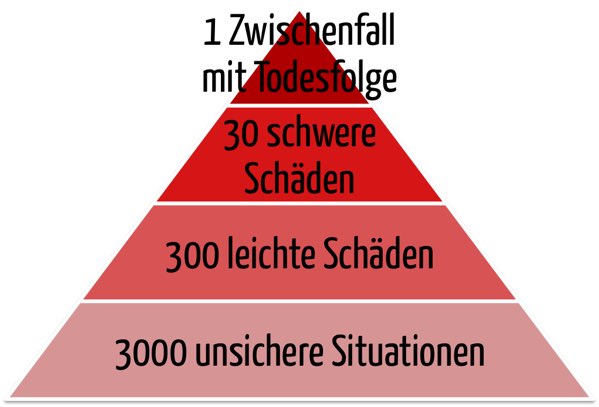
CIRS (Critical Incident Reporting System) auch für Hersteller?
CIRS sind seit Jahren im Gesundheitswesen und der Luftfahrt gesetzlich vorgeschrieben, um Meldungen über kritische Vorkommnisse anonym sammeln, auswerten und daraus Schlüsse für ein sichereres Arbeiten ziehen zu können. Bei Medizinprodukteherstellern sind CIRS keine Pflicht. Ein Fehler? Lesen Sie, wie Sie als Medizinproduktehersteller von CIRS profitieren können.