Software-Lebenszyklus: Was ist damit gemeint?
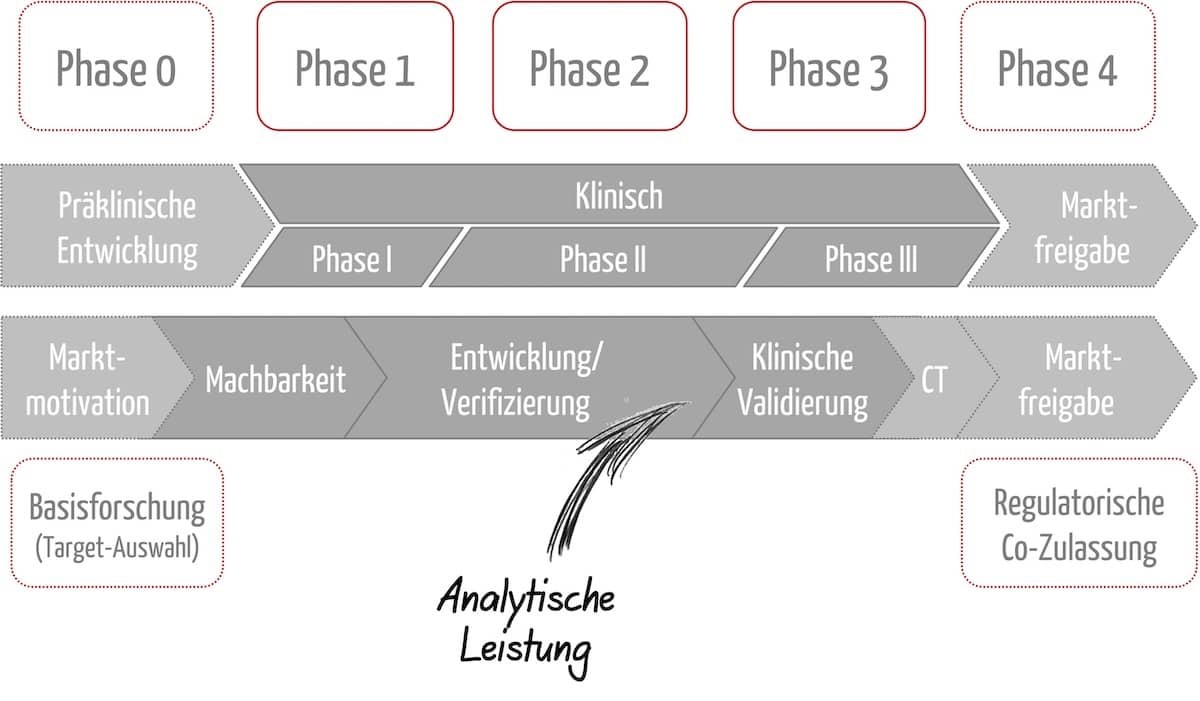
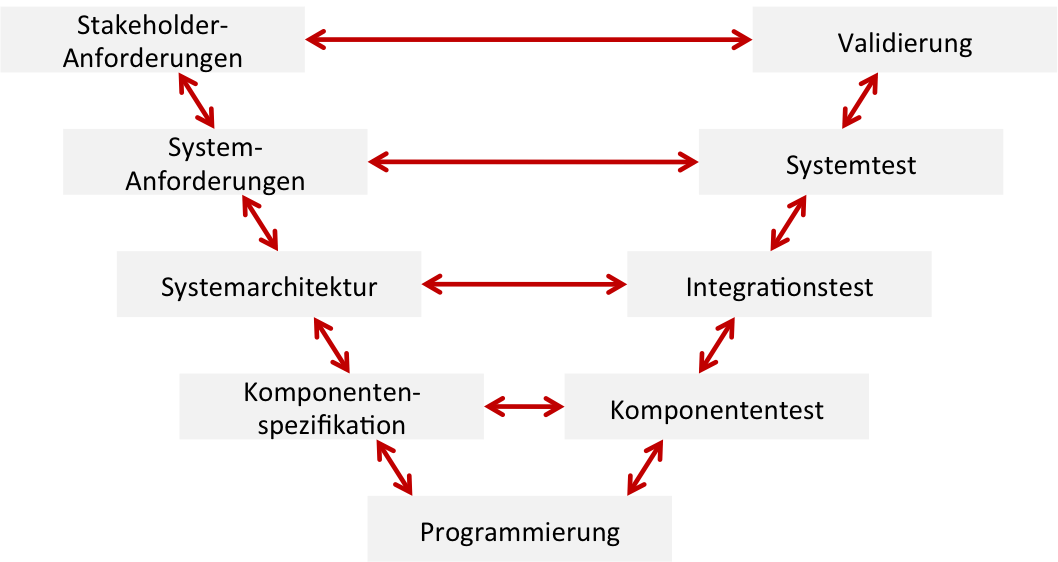
Die Medizinprodukteverordnung (MDR) (wie bereits die Medizinprodukterichtlinie (MDD) und damit das Medizinproduktegesetz zuvor) verlangt, dass Hersteller für ihre Software Lebenszyklus-Prozesse einhalten. Auch die IEC 62304 und die IEC 82304 sprechen von Software-Lebenszyklus-Prozessen. Doch was versteht man unter einem Software-Lebenszyklus? Der Software-Lebenszyklus beinhaltet alle Phasen, die ein Software-Produkt von der ersten Idee bis zur Außerbetriebnahme durchläuft.…
Details