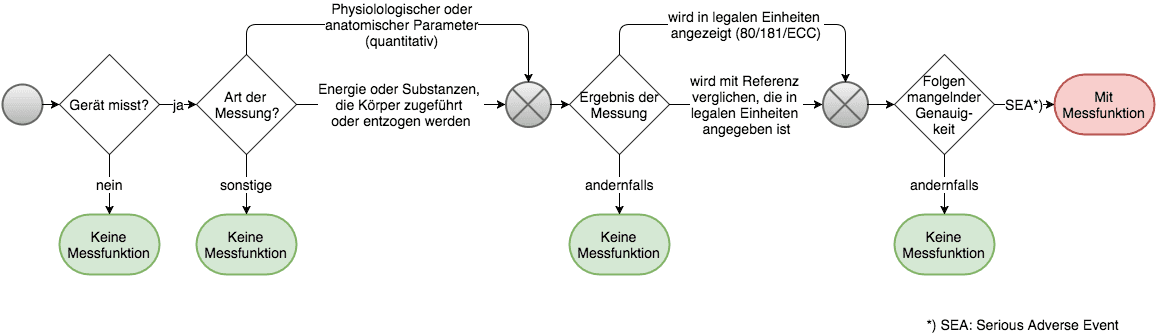
Richtlinie 80/181/EWG: Messeinheiten
Die Richtlinie 80/181/EWG nennt sich Richtlinie „zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über die Einheiten im Messwesen“. Wie alle europäischen Richtlinien bedarf sie einer Überführung in nationales Recht, was im Fall von Deutschland durch die Einheitenverordnung und in Österreich durch das Maß- und Eichgesetz erfolgt.