Der Bereich „Regulatory Affairs“ umfasst über 200 Aufgaben, die bei der Entwicklung und Zulassung von Medizinprodukten zu erledigen sind.
Sie finden hier eine Übersicht über die wichtigsten Inhalte, damit Sie Ihr Produkt schnell zulassen können.
Inhalt
Sie finden auf dieser Seite Fachartikel zu diesen Themen:
- Was Regulatory Affairs ist
- Regulatorische Anforderungen
- Zulassung und Dokumentation
- Behörden, Institutionen und Verbänden
- Weitere Themen der Regulatory Affairs
1. Was Regulatory Affairs ist
Regulatory Affairs umfasst die Prozesse und Aktivitäten, die sicherstellen, dass Medizinprodukte die regulatorischen Anforderungen der Länder erfüllen, in denen sie verkauft werden sollen. Dazu gehören die
- Einholung der erforderlichen Genehmigungen und Freigaben von den Aufsichtsbehörden,
- Einhaltung der geltenden Vorschriften und Normen sowie
- Aufrechterhaltung der Konformität während des gesamten Produktlebenszyklus bis zur Außerbetriebnahme.
Zu den Aufgaben des Bereichs Regulatory Affairs gehört auch die Überwachung von Änderungen der Vorschriften und Normen und die Kommunikation dieser Änderungen mit den Interessengruppen innerhalb des Unternehmens, um eine kontinuierliche Einhaltung zu gewährleisten.
Damit spielt Regulatory Affairs eine entscheidende Rolle, wenn es darum geht, sicherzustellen, dass Medizinprodukte sicher und wirksam sind und den gesetzlichen Anforderungen entsprechen.
2. Regulatorische Anforderungen
a) Deutschland
b) Europa
c) USA
d) Andere Märkte
3. Zulassung und Dokumentation
a) Zulassung
Finden Sie weitere Informationen zur internationalen Zulassung.
b) Qualifizierung und Klassifizierungen (Wie ist mein Produkt einzuteilen?)
c) Technische Dokumentation (Was muss ich pro Produkt dokumentieren?)
d) Qualitätsmanagement (Was sollte Ihre Firma erfüllen?)
Das Qualitätsmanagement zählt üblicherweise nicht zur Verantwortung von Regulatory Affairs. Dennoch listen wir Ihnen einige wichtige Artikel.
4. Behörden, Institutionen und Verbände
a) Deutschland
| BfArM: Bundesamt für Arzneimittel und Medizinprodukte |
| DIMDI (Deutsches Institut für medizinische Informatik; wurde inzwischen in das BfArM integriert) |
| DAkkS, die deutsche Akkreditierungsstelle |
| Länderbehörden: Regierungspräsidien, Gewerbeaufsichtsämter, Regierungen |
b) Europa
c) International
| IMDRF: International Medical Device Regulators Forum |
5. Regulatory Affairs: Weitere Themen
Sie finden hier einen Artikel über die Aufgaben und Kompetenzen von Regulatory Affairs Manager.
Beachten Sie die Vor- und Nachteile von Regulatory Information Management Systemen (RIMS) und deren Rolle bei der digitalen Transformation der Hersteller.
Ein Teil der Aufgaben von Regulatory Affairs ist die Regulatory Intelligence.
Wenn regulatorische Anforderungen nicht erfüllt sind, ist häufig eine Remediation erforderlich.
Benötigen Sie Unterstützung?
Haben Sie noch Fragen, beispielsweise zur Zulassung Ihrer Produkte? Dann nutzen Sie das kostenfreie Micro-Consulting.
Falls Sie Unterstützung dabei wünschen, Ihre Medizinprodukte gesetzeskonform zu entwickeln und „zuzulassen“, dann nehmen Sie gleich Kontakt auf. Das Team das Johner Instituts hilft gerne!
Die Medizinproduktebetreiber-Verordnung (MPBetreibV) fordert in §7 ein Medizinproduktebuch. Betrifft Sie das als Hersteller, wenn Sie für Ihre App Daten auf einem Server speichern? Betrifft das Ihre Kunden, wenn Ihr Medizinprodukt eine standalone Software ist? Finden Sie hier Antworten.
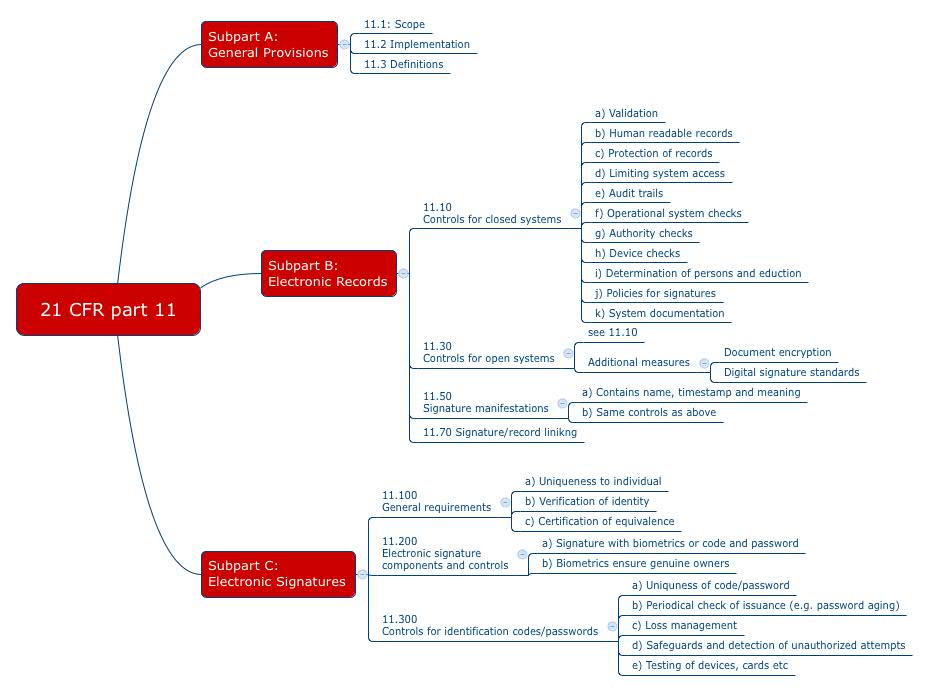
Mit dem 21 CFR part 11 formuliert die FDA Anforderungen an die elektronischen Aufzeichnungen und Unterschriften, die sich auch an Medizinproduktehersteller richten. Viele Firmen drucken alles auf Papier aus und unterschreiben dann mit Hand, um diese Anforderungen des „part 11“ zu umgehen. Ist das wirklich notwendig?
Weiterlesen
Die Forderung nach „Design Verification“ erhebt keinesfalls nur die FDA. Dieser Beitrag beschreibt, was unter „Design Verification“ zu verstehen ist und welche regulatorischen Forderungen Sie als Medizinproduktehersteller erfüllen sollten. Inhaltsübersicht Definition » Regulatorische Anforderungen » Praktische Umsetzung »
Weiterlesen
MDD gilt nicht mehr! Beachten Sie, dass die MDD mit dem 26.05.21 außer Kraft gesetzt und durch die Medizinprodukteverordnung (2017/745) – MDR abgelöst wurde. Unter „MDD Checkliste“ versteht man eine typischerweise tabellarische Auflistung, mit der Medizinprodukte-Hersteller aufzeigen, wie sie die grundlegenden Anforderungen der Richtlinien erfüllen. Inhaltsübersicht MDD Checkliste: Wirklich vorgeschrieben? » Aufbau und Format einer MDD…
Weiterlesen
Den Begriff „Design Validation“ assoziieren die meisten Medizinproduktehersteller mit der FDA. Doch nicht nur die FDA, sondern auch die europäischen Regularien, insbesondere die ISO 13485, fordern eine Validierung von Design und Entwicklung. Inhaltsübersicht Begriffsdefinitionen » Regulatorische Anforderungen » Design Validation bei Software » Eine weiterer häufiger Fehler bei Software-Entwicklern besteht darin, die „Design Validation“ mit der…
Weiterlesen
Die NBOG ist die Notified Body Operations Group. Diese Organisation legt Richtlinien fest, von denen Sie als Hersteller zumindest indirekt betroffen sind.
Weiterlesen
Ein Review ist eine manuelle Bewertung eines Artefakts (z.B. Code, Dokument), das abhängig von den formalen Anforderungen und den beteiligten Personen beispielsweise als Inspektion oder Walk-through bezeichnet wird.
Moderne eHealth-Sensoren sind für wenig Geld zu haben. Etablierte Medizinproduktehersteller belächeln diese Produkte, schließlich sei es ein langer Weg von einer eHealth-Sensor-Plattform zu einem Medizinprodukt. Alleine der Overhead für die „Zulassung“ und die Dokumentation für all die Normen sei unendlich viel Arbeit. Update Im Rahmen eines Forschungsprojekts werden wir untersuchen, wie hoch der Aufwand tatsächlich…
Weiterlesen
Die FDA MAUDE Datenbank stellt Informationen zur „Manufacturer and User Facility Device Experience“ bereit. Sie entspricht damit etwa der Datenbank, mit der das BfArM Meldungen von Hersteller zur Risiken publiziert. Inhaltsübersicht Inhalt der MAUDE Datenbank » Neues Werkzeug zur Auswertung » Regulatorischer Hintergrund »
Weiterlesen
Unter der „Refuse to Accept Policy“ der FDA versteht man einen Kriterienkatalog, anhand dessen die FDA 510(k) Anträge bewertet und ggf. zurückweist. Diese „Refuse to Accept Policy“ hat die FDA im August 2015 aktualisiert.