Der Bereich „Regulatory Affairs“ umfasst über 200 Aufgaben, die bei der Entwicklung und Zulassung von Medizinprodukten zu erledigen sind.
Sie finden hier eine Übersicht über die wichtigsten Inhalte, damit Sie Ihr Produkt schnell zulassen können.
Inhalt
Sie finden auf dieser Seite Fachartikel zu diesen Themen:
- Was Regulatory Affairs ist
- Regulatorische Anforderungen
- Zulassung und Dokumentation
- Behörden, Institutionen und Verbänden
- Weitere Themen der Regulatory Affairs
1. Was Regulatory Affairs ist
Regulatory Affairs umfasst die Prozesse und Aktivitäten, die sicherstellen, dass Medizinprodukte die regulatorischen Anforderungen der Länder erfüllen, in denen sie verkauft werden sollen. Dazu gehören die
- Einholung der erforderlichen Genehmigungen und Freigaben von den Aufsichtsbehörden,
- Einhaltung der geltenden Vorschriften und Normen sowie
- Aufrechterhaltung der Konformität während des gesamten Produktlebenszyklus bis zur Außerbetriebnahme.
Zu den Aufgaben des Bereichs Regulatory Affairs gehört auch die Überwachung von Änderungen der Vorschriften und Normen und die Kommunikation dieser Änderungen mit den Interessengruppen innerhalb des Unternehmens, um eine kontinuierliche Einhaltung zu gewährleisten.
Damit spielt Regulatory Affairs eine entscheidende Rolle, wenn es darum geht, sicherzustellen, dass Medizinprodukte sicher und wirksam sind und den gesetzlichen Anforderungen entsprechen.
2. Regulatorische Anforderungen
a) Deutschland
b) Europa
c) USA
d) Andere Märkte
3. Zulassung und Dokumentation
a) Zulassung
Finden Sie weitere Informationen zur internationalen Zulassung.
b) Qualifizierung und Klassifizierungen (Wie ist mein Produkt einzuteilen?)
c) Technische Dokumentation (Was muss ich pro Produkt dokumentieren?)
d) Qualitätsmanagement (Was sollte Ihre Firma erfüllen?)
Das Qualitätsmanagement zählt üblicherweise nicht zur Verantwortung von Regulatory Affairs. Dennoch listen wir Ihnen einige wichtige Artikel.
e) Regulatorische Rollen
Sie finden hier Fachartikel zu mehreren regulatorischen Rollen;
4. Behörden, Institutionen und Verbände
a) Deutschland
| BfArM: Bundesamt für Arzneimittel und Medizinprodukte |
| DIMDI (Deutsches Institut für medizinische Informatik; wurde inzwischen in das BfArM integriert) |
| DAkkS, die deutsche Akkreditierungsstelle |
| Länderbehörden: Regierungspräsidien, Gewerbeaufsichtsämter, Regierungen |
b) Europa
c) International
| IMDRF: International Medical Device Regulators Forum |
5. Regulatory Affairs: Weitere Themen
Die Aufgaben von Regulatory Affairs umfassen auch das Finden und Beseitigen von Abweichungen und Nicht-Konformitäten. Die (notfallmäßige) Beseitigung nennt sich Remediation.
Beachten Sie die Vor- und Nachteile von Regulatory Information Management Systemen (RIMS) und deren Rolle bei der digitalen Transformation der Hersteller.
Ein Teil der Aufgaben von Regulatory Affairs ist die Regulatory Intelligence.
Benötigen Sie Unterstützung?
Haben Sie noch Fragen, beispielsweise zur Zulassung Ihrer Produkte? Dann nutzen Sie das kostenfreie Micro-Consulting.
Falls Sie Unterstützung dabei wünschen, Ihre Medizinprodukte gesetzeskonform zu entwickeln und „zuzulassen“, dann nehmen Sie gleich Kontakt auf. Das Team das Johner Instituts hilft gerne!
Ein CB Report ist ein Prüfbericht, der von einem akkreditierten CB Testlabor (CBTL) erstellt wird. Er kann als Grundlage für nationale Zertifizierungen und Zulassungen dienen. Test- und Prüflabore wie zahlreiche TÜVs oder der VDE bieten Prüfungen konform mit dem „CB Scheme“ an. Sie erstellen als Ergebnis solche CB Reports. Wann Medizinproduktehersteller diese CB Reports überhaupt benötigen, erfahren Sie…
Details
Wann zählt ein PC zur Medical IT, wann als Medizinprodukt? Die Antwort auf diese Fragen hat weitgehende regulatorische Konsequenzen.
Besonders große Medizintechnik-Hersteller nutzen das Outsourcing, um Teile der Wertschöpfungskette auszulagern. Verschaffen Sie sich in diesem Artikel einen Überblick über die Chancen und Risiken des Outsourcings und über die Besonderheiten bei Medizinprodukten.
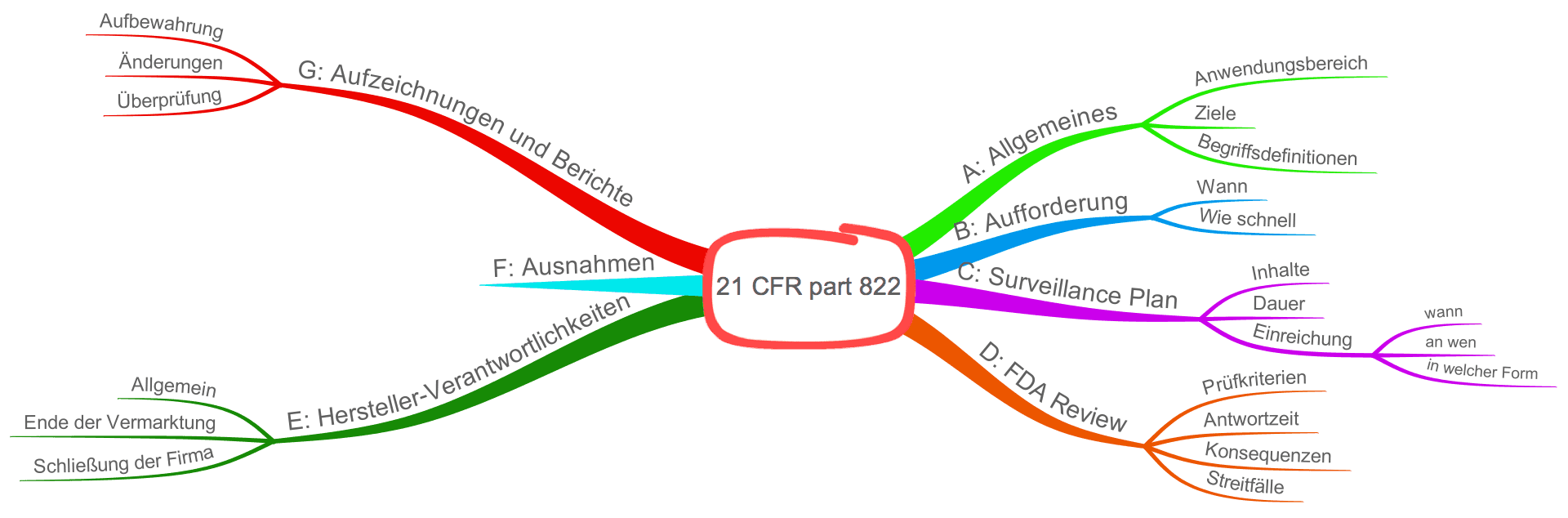
Mit dem 21 CFR part 822 legt die FDA die Anforderungen an die Post-Market Surveillance fest. Ein zugehöriges „Guidance Document“ gibt Handlungsleitung, wie Hersteller die Forderungen des 21 CFR part 822 erfüllen sollen.
Die Richtlinie 80/181/EWG nennt sich Richtlinie „zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über die Einheiten im Messwesen“. Wie alle europäischen Richtlinien bedarf sie einer Überführung in nationales Recht, was im Fall von Deutschland durch die Einheitenverordnung und in Österreich durch das Maß- und Eichgesetz erfolgt.
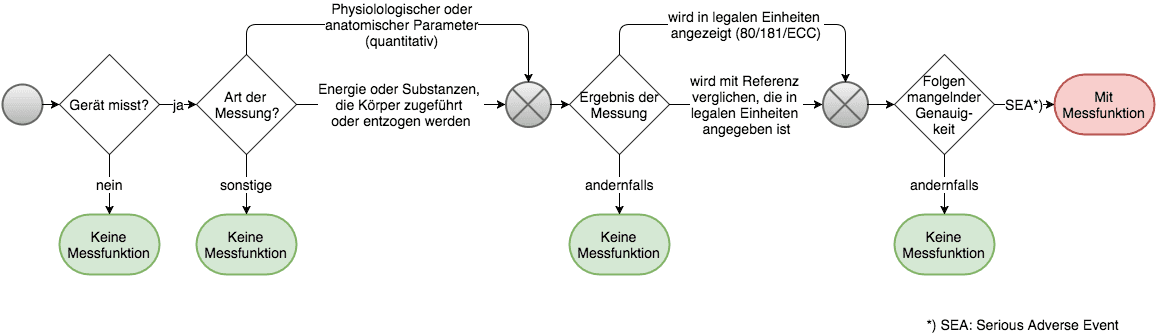
Medizinprodukte mit Messfunktion sind etwas Besonderes. Wichtig (u.a.): Messfunktion beeinflusst die Klassifizierung. Doch nicht alles, was misst, hat eine Messfunktion. Bei der Einordnung hilft die MEDDEV 2.1./5.
Die Health Breach Notification Rule legt fest, wann Anbieter von Health Records welche Probleme mit der Datensicherheit an wen, in welcher Frist und in welcher Form melden müssen. Dieser Artikel verschafft Ihnen eine schnelle Übersicht über die Forderung der US-amerikanischen Federal Trace Commission (FTC).
Die Federal Trade Commission (FTC) ist eine US-amerikanische Behörde, deren Zielsetzung in der Wahrung des Wettbewerbsrechts und des Verbraucherschutzes liegt. Unter welchen Umständen Sie auch die Anforderungen der FTC beachten müssen und worin diese Anforderungen bestehen, lesen Sie in diesem Beitrag. Wie radikal die FTC auch bei Herstellern von Medical Apps vorgehen kann, zeigt der Fall Lumosity.
Details
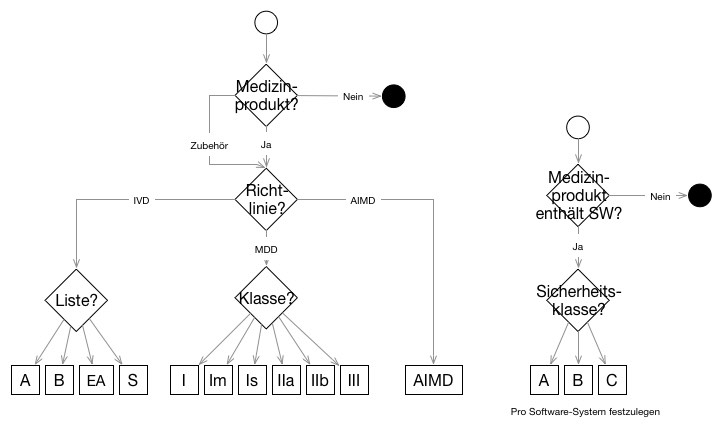
Der Begriff Klassifizierung ist bei Medizinprodukten mehrfach belegt: Die erste Klassifizierung betrifft die Abgrenzung von Medizinprodukten, Nicht-Medizinprodukten und Zubehör zu Medizinprodukten. Die nächste Klassifizierung bezieht sich auf den Typ von Medizinprodukten bzw. der anzuwendenden EU-Richtlinien, konkret die MDD, die IVD und die AIMD. Einige Richtlinien definieren selbst wieder Klassen wie die Klassen I, IIa, IIb und III bei der MDD. Unabhängig davon…
Details
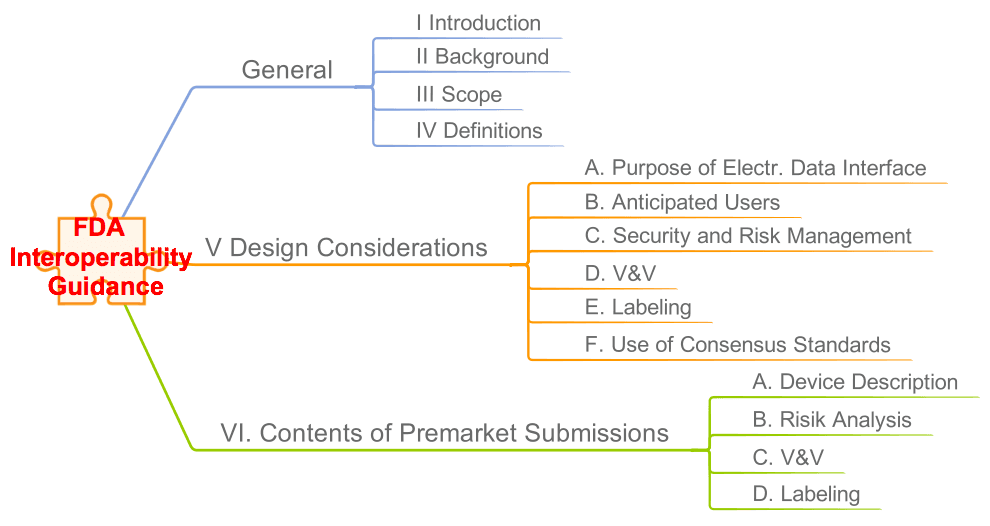
Die FDA hat ein Interoperability Guidance als Entwurf veröffentlicht. Es trägt den Titel „Design Considerations and Pre-market Submission Recommendations for Interoperable Medical Devices“ (hier zum Download). Lesen Sie hier, was die FDA damit bezweckt und auf welche Anforderungen Sie sich einstellen müssen.
Details