Der Bereich „Regulatory Affairs“ umfasst über 200 Aufgaben, die bei der Entwicklung und Zulassung von Medizinprodukten zu erledigen sind.
Sie finden hier eine Übersicht über die wichtigsten Inhalte, damit Sie Ihr Produkt schnell zulassen können.
Inhalt
Sie finden auf dieser Seite Fachartikel zu diesen Themen:
- Was Regulatory Affairs ist
- Regulatorische Anforderungen
- Zulassung und Dokumentation
- Behörden, Institutionen und Verbänden
- Weitere Themen der Regulatory Affairs
1. Was Regulatory Affairs ist
Regulatory Affairs umfasst die Prozesse und Aktivitäten, die sicherstellen, dass Medizinprodukte die regulatorischen Anforderungen der Länder erfüllen, in denen sie verkauft werden sollen. Dazu gehören die
- Einholung der erforderlichen Genehmigungen und Freigaben von den Aufsichtsbehörden,
- Einhaltung der geltenden Vorschriften und Normen sowie
- Aufrechterhaltung der Konformität während des gesamten Produktlebenszyklus bis zur Außerbetriebnahme.
Zu den Aufgaben des Bereichs Regulatory Affairs gehört auch die Überwachung von Änderungen der Vorschriften und Normen und die Kommunikation dieser Änderungen mit den Interessengruppen innerhalb des Unternehmens, um eine kontinuierliche Einhaltung zu gewährleisten.
Damit spielt Regulatory Affairs eine entscheidende Rolle, wenn es darum geht, sicherzustellen, dass Medizinprodukte sicher und wirksam sind und den gesetzlichen Anforderungen entsprechen.
2. Regulatorische Anforderungen
a) Deutschland
b) Europa
c) USA
d) Andere Märkte
3. Zulassung und Dokumentation
a) Zulassung
Finden Sie weitere Informationen zur internationalen Zulassung.
b) Qualifizierung und Klassifizierungen (Wie ist mein Produkt einzuteilen?)
c) Technische Dokumentation (Was muss ich pro Produkt dokumentieren?)
d) Qualitätsmanagement (Was sollte Ihre Firma erfüllen?)
Das Qualitätsmanagement zählt üblicherweise nicht zur Verantwortung von Regulatory Affairs. Dennoch listen wir Ihnen einige wichtige Artikel.
e) Regulatorische Rollen
Sie finden hier Fachartikel zu mehreren regulatorischen Rollen;
4. Behörden, Institutionen und Verbände
a) Deutschland
| BfArM: Bundesamt für Arzneimittel und Medizinprodukte |
| DIMDI (Deutsches Institut für medizinische Informatik; wurde inzwischen in das BfArM integriert) |
| DAkkS, die deutsche Akkreditierungsstelle |
| Länderbehörden: Regierungspräsidien, Gewerbeaufsichtsämter, Regierungen |
b) Europa
c) International
| IMDRF: International Medical Device Regulators Forum |
5. Regulatory Affairs: Weitere Themen
Die Aufgaben von Regulatory Affairs umfassen auch das Finden und Beseitigen von Abweichungen und Nicht-Konformitäten. Die (notfallmäßige) Beseitigung nennt sich Remediation.
Beachten Sie die Vor- und Nachteile von Regulatory Information Management Systemen (RIMS) und deren Rolle bei der digitalen Transformation der Hersteller.
Ein Teil der Aufgaben von Regulatory Affairs ist die Regulatory Intelligence.
Benötigen Sie Unterstützung?
Haben Sie noch Fragen, beispielsweise zur Zulassung Ihrer Produkte? Dann nutzen Sie das kostenfreie Micro-Consulting.
Falls Sie Unterstützung dabei wünschen, Ihre Medizinprodukte gesetzeskonform zu entwickeln und „zuzulassen“, dann nehmen Sie gleich Kontakt auf. Das Team das Johner Instituts hilft gerne!
Mit dem UDI-System hat die EU eine Pflicht zur Identifikation und Registrierung von Medizinprodukten eingeführt, die weit über das unter der MDD noch Geforderte hinausgeht. Selbst für Standalone-Software fordert die Medical Device Regulation MDR eine UDI. Lesen Sie hier, worauf Sie sich vorbereiten müssen.
Details
Das Premarket Approval (PMA-Verfahren) müssen v. a. Hersteller von Medizinprodukten der Klasse III durchlaufen. Es ist das aufwändigste „Zulassungsverfahren“ der FDA, dessen typische Bearbeitungszeit länger als ein Jahr beträgt. Die FDA genehmigt pro Jahr meist nur wenige Dutzend PMA-Anträge. Dieser Fachartikel stellt die Anforderungen der FDA vor und gibt Tipps, wie Hersteller diese hohe Hürde dennoch…
Details
Welche regulatorischen Anforderungen Hersteller erfüllen müssen, wie sich ein Vigilanz-System von einem System für die Post-Market Surveillance unterscheidet und wie Firmen ein Vigilanz-System schnell und gesetzeskonform aufbauen und betreiben, erklärt dieser Beitrag.
Die europäische Medical Device Regulation MDR (EU-Medizinprodukteverordnung) müssen Hersteller beachten, die Medizinprodukte in der EU in den Verkehr bringen wollen. Diese Verordnung (EU) 2017/745 über Medizinprodukte, so der offizielle Titel, stellt auch Anforderungen an Benannte Stellen, Händler, Importeure und Gesundheitseinrichtungen wie Krankenhäuser.
Details
Die DAkkS, die Deutsche Akkreditierungsstelle, ist die nationale Akkreditierungsbehörde der Bundesrepublik Deutschland.
In diesem Beitrag erfahren Sie,
Eine Interessenerklärung (engl. Declaration of Interest) ist ein formales Dokument, das dazu dient, potenzielle Interessenkonflikte transparent zu machen. Durch die Abgabe einer Interessenerklärung möchten Personen ihre Objektivität und Unabhängigkeit demonstrieren. In diesem Artikel geht es um Interessenerklärungen im klinischen Kontext.
Details
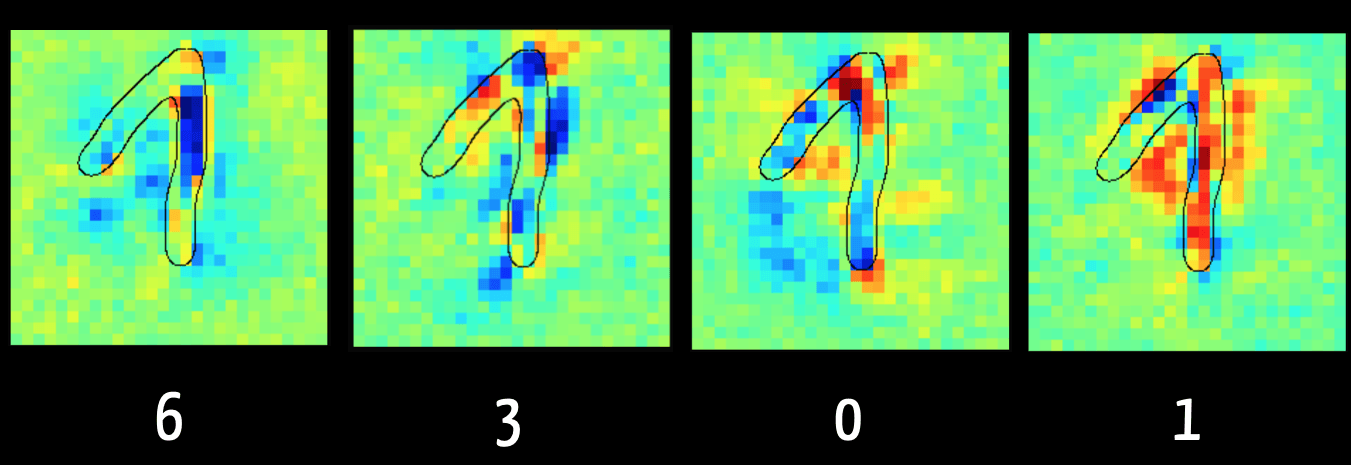
Immer mehr Medizinprodukte nutzen künstliche Intelligenz, um Krankheitsbilder präziser zu diagnostizieren und Patienten wirksamer zu behandeln.
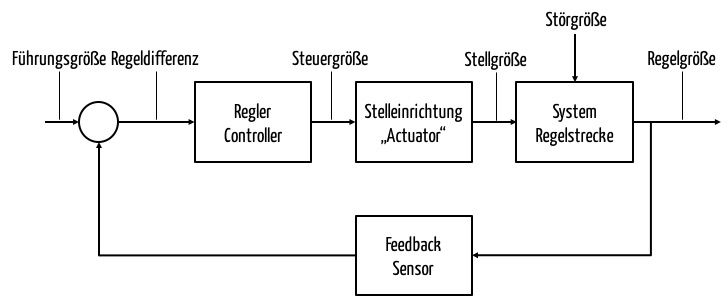
Medizinprodukte basieren zunehmend auf Closed-Loop-Systemen. Diese „geschlossenen Regelsysteme“ finden bereits in der Medizinprodukteverordnung MDR Erwähnung. Ein Beispiel ist ein System aus einer Insulinpumpe, die von einem Gerät mit Glukosesensor gesteuert wird. Sie erfahren in diesem Artikel, was Closed-Loop-Systeme sind, wo sie in der Medizin zum Einsatz kommen und welche regulatorischen Anforderungen sie erfüllen müssen. Der…
Details
Die Einteilung, ob ein Produkt ein Arzneimittel oder ein stoffliches Medizinprodukt ist, hat weitreichende regulatorische Folgen. Diese Einteilung ist so anspruchsvoll, dass es regelmäßig Dispute mit Behörden und Benannten Stellen gibt und 2023 sogar der EuGH dazu urteilen musste. Dieser Artikel hilft Herstellern, Behörden und Benannten Stellen bei der „Qualifizierung“ eines Produkts. Er geht auf…
Details